Все мы знаем, что движение — жизнь. И многие из нас знают, что процесс эволюции создал нас идеальными бегунами на длинные дистанции. Как и за счет чего у нас получается двигаться и делать это долго, а зачастую еще и быстро? Всё устроено примерно так: для движения нужна энергия, а для получения энергии нужны кислород и пища. Но как из воды, еды и кислорода получается энергия, используемая для различных нужд организма? Здесь в дело вступает наш самый главный, но невидимый союзник — митохондрия.
- Что такое митохондрии?
- АТФ и его роль в клетке. Функции митохондрий клетки
- Строение митохондрий и их функции
- Объем или интенсивность?
- Как работает валюта под названием АТФ?
- Вода и еда?
- Больше тренировок — больше митохондрий?
- Можем ли мы влиять на митохондрии?
- Зачем нам кислород?
- Каким образом митохондрии вырабатывают энергию?
- «Как белка в колесе» — динамика митохондрий
- Здоровые циклы деления и слияния – залог метаболического здоровья клетки
- Митофузины – не просто какие-то белки
- Гипоталамус, митохондрии, метаболическая дисфункция и старение
- Так кто и как регулирует чувствительность нейронов гипоталамуса?
- Как повлиять на динамику митохондрий?
- Генная терапия митохондрий
- Перенос митохондрий
- Много митохондрий не бывает (вместо вывода)
Что такое митохондрии?
Слово «митохондрия» постоянно встречается в литературе, посвященной спорту на выносливость, и это неспроста. Почему и зачем маленькой митохондрии уделяется столько внимания?
Митохондрии — это маленькие (размером с 1/2000–1/4000-ю часть кончика иголки) внутриклеточные органеллы, наши миниатюрные энергетические станции, которых в теле человека содержится огромное количество — примерно 2000 митохондрий на одну клетку. Это самый трудолюбивый и, наверно, самый прожорливый компонент клетки.
Любопытен факт происхождения митохондрии. В 1926 году ученый по имени Айвен Уоллин выдвинул предположение, что митохондрии когда-то были самостоятельно живущими бактериями, а в процессе эволюции стали частью нашего организма. На роль «отца» митохондрии в 1985 году группа ученых номинировала микроорганизм со сложным названием Alphaproteobacteria. К слову, даже находясь внутри человеческой клетки, митохондрия продолжает вести вполне самостоятельную жизнь: у нее есть своя «мастерская» по синтезу белка, включая и собственные молекулы ДНК и РНК.

АТФ и его роль в клетке. Функции митохондрий клетки
Основным источником энергии для клетки являются питательные вещества: углеводы, жиры и белки, которые окисляются с помощью кислорода. Практически все углеводы, прежде чем достичь клеток организма, благодаря работе желудочно-кишечного тракта и печени превращаются в глюкозу. Наряду с углеводами расщепляются также белки — до аминокислот и липиды — до жирных кислот.В клетке питательные вещества окисляются под действием кислорода и при участии ферментов, контролирующих реакции высвобождения энергии и ее утилизацию.
Почти все окислительные реакции происходят в митохондриях, а высвобождаемая энергия запасается в виде макроэргического соединения — АТФ. В дальнейшем для обеспечения внутриклеточных метаболических процессов энергией используется именно АТФ, а не питательные вещества.
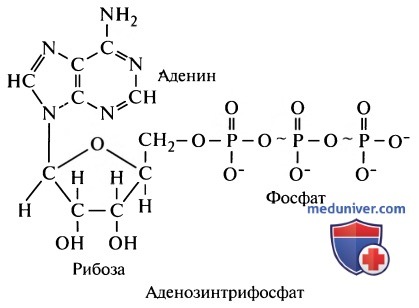
Молекула АТФ содержит: (1) азотистое основание аденин; (2) пентозный углевод рибозу, (3) три остатка фосфорной кислоты. Два последних фосфата соединены друг с другом и с остальной частью молекулы макроэргическими фосфатными связями, обозначенными на формуле АТФ символом ~. При соблюдении характерных для организма физических и химических условий энергия каждой такой связи составляет 12000 калорий на 1 моль АТФ, что во много раз превышает энергию обычной химической связи, поэтому фосфатные связи и называют макроэргическими. Более того, эти связи легко разрушаются, обеспечивая внутриклеточные процессы энергией сразу, как только в этом возникает необходимость.
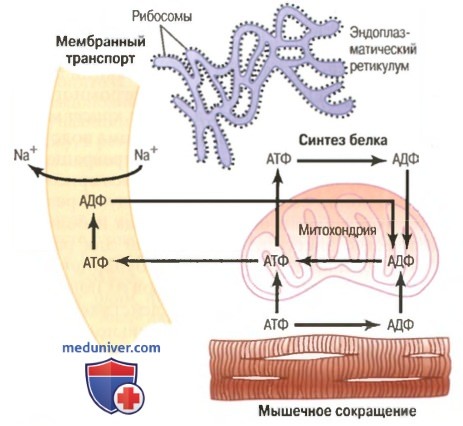
При высвобождении энергии АТФ отдает фосфатную группу и превращается в аденозиндифосфат. Выделившаяся энергия используется практически для всех клеточных процессов, например в реакциях биосинтеза и при мышечном сокращении.
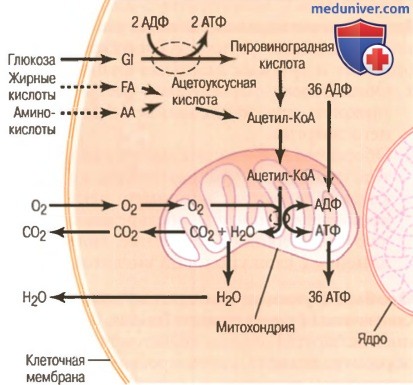
Схема образования аденозинтрифосфата в клетке, показывающая ключевую роль митохондрий в этом процессе.
GI – глюкоза; FA – жирные кислоты; АА – аминокислота.
Восполнение запасов АТФ происходит путем воссоединения АДФ с остатком фосфорной кислоты за счет энергии питательных веществ. Этот процесс повторяется вновь и вновь. АТФ постоянно расходуется и накапливается, поэтому она получила название энергетической валюты клетки. Время оборота АТФ составляет всего несколько минут.
Роль митохондрий в химических реакциях образования АТФ. При попадании внутрь клетки глюкоза под действием ферментов цитоплазмы превращается в пировиноградную кислоту (этот процесс называют гликолизом). Энергия, высвобождаемая в этом процессе, затрачивается на превращение небольшого количества АДФ в АТФ, составляющего менее 5% общих запасов энергии.
Синтез АТФ на 95% осуществляется в митохондриях. Пировиноградная кислота, жирные кислоты и аминокислоты, образующиеся соответственно из углеводов, жиров и белков, в матриксе митохондрий в итоге превращаются в соединение под названием «ацетил-КоА». Это соединение, в свою очередь, вступает в серию ферментативных реакций под общим названием «цикл трикарбоновых кислот» или «цикл Кребса», чтобы отдать свою энергию.
В цикле трикарбоновых кислот ацетил-КоА расщепляется до атомов водорода и молекул углекислого газа. Углекислый газ удаляется из митохондрий, затем — из клетки путем диффузии и выводится из организма через легкие.
Атомы водорода химически очень активны и поэтому сразу вступают в реакцию с кислородом, диффундирующим в митохондрии. Большое количество энергии, выделяющейся в этой реакции, используется для превращения множества молекул АДФ в АТФ. Эти реакции достаточно сложны и требуют участия огромного числа ферментов, входящих в состав крист митохондрий. На начальном этапе от атома водорода отщепляется электрон, и атом превращается в ион водорода. Процесс заканчивается присоединением ионов водорода к кислороду. В результате этой реакции образуются вода и большое количество энергии, необходимой для работы АТФ-синтетазы — крупного глобулярного белка, выступающего в виде бугорков на поверхности крист митохондрий. Под действием этого фермента, использующего энергию ионов водорода, АДФ превращается в АТФ. Новые молекулы АТФ направляются из митохондрий ко всем отделам клетки, включая ядро, где энергия этого соединения используется для обеспечения самых разных функций.
Данный процесс синтеза АТФ в целом называют хемиосмотическим механизмом образования АТФ.
Строение митохондрий и их функции
– Также рекомендуем “Как используется АТФ клеткой? Амебоидное движение клетки”
Объем или интенсивность?
Как стало понятно, регулярные тренировки — наилучший способ повлиять на митохондрии. Но что выбрать — объем или интенсивность? Правильный ответ — и то и другое. Давайте разберемся, как влияют на митохондрии повышение тренировочного объема и увеличение интенсивности.
Как работает валюта под названием АТФ?
Каким образом АТФ помогает нам быть быстрее, выше, сильнее? Конечно, с помощью мышц. Внутри каждой мышечной клетки есть микроскопические нити протеина — актин и миозин. АТФ прикрепляется к миозину и помогает ему «зацепиться» за актин, перемещаясь и вызывая сокращение мышцы. Если по какой-то причине (недостаток кислорода или глюкозы) АТФ в вашем организме будет недостаточно — мышцы не смогут эффективно сокращаться, и вы довольно сильно замедлитесь или даже остановитесь. Знакомая ситуация?
Продукция энергии в мышцах — сложный и комплексный процесс, но для него требуются простые ингредиенты, а именно сахар, кислород и кальций. Сахар — поставщик основных строительных блоков (пируват и НАД) для митохондрий, из которых получится АТФ. Кислород нужен для эффективного производства клеточной «валюты». Кальций помогает глюкозе трансформироваться в пируват и НАД, а также облегчает взаимодействие актина и миозина, помогая мышце сокращаться.

Вода и еда?
Оптимальная функция клеток и внутриклеточных структур невозможна без поддержания оптимального водно-электролитного баланса, а также регулярного поступления питательных веществ, в частности углеводов. Внимательно следите за тем, чтобы пить достаточное количество воды, а также соблюдайте сбалансированную диету, чтобы обеспечить организм необходимыми строительными материалами.
Больше тренировок — больше митохондрий?
Важно соблюдать баланс в тренировках, так как перетренированность и регулярные тренировки без должного восстановления приводят к повреждению мышечных клеток, включая и митохондрии. Вовремя заметить и не допустить перетренированности, а также оценить качество восстановления можно также с помощью пульсометра, путем наблюдения за пульсом покоя или вариабельностью пульса.

Можем ли мы влиять на митохондрии?
Давайте перейдем от теоретических рассуждений к практике. Можем ли мы в реальной жизни влиять на работу митохондрий и, если да, как это сделать?
Самое интересное, что мы довольно легко можем увеличить количество митохондрий в нашем организме и даже улучшить качество их работы. И сделать это нам помогают регулярные аэробные тренировки.
В июльском номере журнала Sports Medicine авторы проследили связь между регулярными тренировками и количеством митохондрий. Оказалось, что аэробные нагрузки влияют на процесс образования митохондрий довольно предсказуемым образом: чем больше вы тренируетесь, тем больше митохондрий образуется. В течение нескольких месяцев количество митохондрий может увеличиться на 50%, но верно и обратное — как только регулярные тренировки прекращаются, количество митохондрий уменьшается, возвращаясь к исходным базовым значениям в течение нескольких месяцев.
Зачем нам кислород?
Простой вопрос, но очень часто вызывает недоумение даже у студентов-медиков. Правильный ответ: кислород нужен митохондриям для производства АТФ. Без кислорода невозможна эффективная работа и производство АТФ. При достаточном его наличии скорость выработки АТФ в мышцах примерно в 13 раз выше, чем в ситуации недостаточного снабжения митохондрий кислородом. Говоря о недостатке кислорода и недостаточной выработке АТФ, нужно понимать, что речь идет не столько о нахождении, скажем, в условиях разреженного воздуха гор, а прежде всего о чрезмерно интенсивных (и частых) тренировках выше так называемого «лактатного порога». Каждый раз, проводя такую жесткую тренировку, мы залезаем в кислородный долг у организма, который нужно будет отдавать. Самым надежным способом уберечь себя от накопления этого долга является контроль пульса на тренировках, причем делать это лучше не по ощущениям, а с помощью более точного прибора — пульсометра.
Каким образом митохондрии вырабатывают энергию?
Короткий ответ — при помощи цикла Кребса и переноса электронов в дыхательной цепи. Не пугайтесь! Это значит, что для получения энергии митохондрии используют кислород и углеводы (сахар). Глюкоза, попадая внутрь митохондрии, «переупаковывается» в два важных компонента — пируват и никотинамидадениндинуклеотид (НАД). Эти два вещества транспортируются в центральную часть митохондрии, где в присутствии кислорода (это наиважнейший момент эффективной продукции энергии!) используются для выработки главного энергетического субстрата — АТФ. Правильнее рассматривать АТФ как валюту клетки, которая идет на оплату счетов за свет, воду, газ и электричество.
Время на прочтение
Митохондрии – маленькие труженики или большие начальники?
Если вы думаете, что самая важная для нас история совместной жизни начинается во время свадьбы, то это совсем не так. Самая важная история совместной жизни каждого человека началась более миллиарда лет назад, когда наши далекие одноклеточные предки вынуждены были подписать «брачный контракт» с теми, кого мы сейчас называем митохондрии (см. теория симбиогенеза).
Митохондрии имеют две мембраны (внутреннюю и внешнюю) и собственный наследственный материал в виде ДНК (рис.1). На внутренней мембране митохондрий находится система окислительного фосфорилирования, работа которой обеспечивает окисление энергетических субстратов с образованием АТФ.

Рис. 1. Схематическое строение митохондрии
«Как белка в колесе» — динамика митохондрий
Больше всего митохондрий находится в тканях с высокими энергетическими потребностями, — мышцы, печень, бурая жировая ткань, мозг. Неудивительно, что и динамика митохондрий в этих тканях изучена лучше.
Клеточный метаболический гомеостаз зависит от баланса между потреблением питательных веществ и их расходом. Перемены в поставке питательных веществ приводит к клеточным адаптациям для восстановления баланса. Избыток питания приводит к фрагментации митохондриальной сети, что вызывает снижение биоэнергетической эффективности митохондрий. Это позволит избежать потерь энергии. Напротив, при метаболическом голоде митохондрии удлиняются, чтобы увеличить свою биоэнергетическую эффективность.
В чем хитрость этих движений? Если клетка находится в состоянии голода, то слияние митохондрий позволяет увеличить их биоэнергетическую эффективность (количество АТР, которое создается на молекулу питательного вещества). Если же в клетку поступает избыток питательных веществ, то их можно либо 1) запасти, либо 2)рассеять эту энергию в виде тепла. Задача митохондрий в этом случае, — рассеять больше энергии в виде тепла, запасти меньше в виде АТФ (накопление NADH и АФК приведет к окислительному стрессу). Фрагментация митохондрий позволяет им снизить биоэнергетическую эффективность, главным механизмом снижения которой считается «утечка» протонов.
Так что, мы ходим на работу, а жизнь митохондрий постоянно протекает в режиме цикла деления и слияния (рис 3).
Здоровые циклы деления и слияния – залог метаболического здоровья клетки
Нормальный цикл деления митохондрий и их слияния является ключевым звеном контроля их качества. Почему? При делении митохондрий образуется две дочерние, одна из которых имеет более высокий мембранный потенциал и идет дальше в цикл слияния-деления, а другая, с более деполяризованной мембраной, остается отделенной до восстановления мембранного потенциала. Если потенциал восстанавливается, — она воссоединяется с митохондриальной сетью. Если она остается деполяризованной, то она элиминируется в процессе аутофагии, что является залогом качества пула митохондрий (рис.4).
С другой стороны, избыток питательных веществ приводит к ингибированию слияния митохондрий, что приводит к нарушению цикла митохондриальной динамики, увеличивает внутриклеточную митохондриальную гетерогенность. Да, при избытке еды фрагментация митохондрий протективна, однако длительная фрагментация, как и длительное слияние, вредна для контроля качества митохондрий. Не происходит селективного удаления, митохондриальная масса будет уменьшаться и состоять из небольших деполяризованных митохондрий.
Митофузины – не просто какие-то белки
На молекулярном уровне слияние митохондрий является двухстадийным процессом, который требует координированного слияния внешней и внутренней мембран в ходе отдельных последовательных событий. У млекопитающих этот процесс регулируется тремя белками, которые относятся к GTPазам: Mfn1 и Mfn2 необходимы для слияния внешней мембраны, а ОРА1 – для слияния внутренней мембраны. Для деления нужны другие белки, — Fis1 и Drp1.
Роль белков-митофузинов была изучена в loss- and gain-of function studies. Мышки, мутантные по белкам-митофузинам, погибают еще в mid-gestation, потому что у них невозможным становится слияние митохондрий. Митофузины важны для процессов аутофагии и митофагии. Снижение экспрессии Mfn2 в кардиомиоцитах блокирует запуск процесса аутофагии, потому что блокируется слияние аутофагосом с лизосомами. Истощение Mfn2 приводит к снижению потенциала мембран митохондрий, для компенсации происходит снижение работы дыхательной цепи, возрастает поглощение глюкозы и снижается синтез гликогена. Клетка переходит на анаэробный глиоклиз, а это – путь к онкологическому перерождению клетки. Дефицит Mfn2 приводит к нейродегенеративным изменениям. Повышение экспрессии Mfn2 в скелетных мышцах повышает их чувствительность к инсулину.
Гипоталамус, митохондрии, метаболическая дисфункция и старение
Динамика митохондрий важна во всех клетках. В бета-клетках поджелудочной железы митохондрии являются сенсорами питательных веществ и генераторами сигналов синтеза инсулина, в мышцах динамика митохондрий важна для регуляции метаболизма глюкозы и т.д. Однако человек не просто совокупность клеток разного типа, каждая из которых принимает самостоятельные решения. Организм – это система, у которой есть центральное регуляторное звено поддержания гомеостаза энергии и глюкозы. Этим главным регулятором является гипоталамус.
Гипоталамус расположен в промежуточном мозге и именно он обеспечивает взаимосвязь нервной и гуморальной систем регуляции. Нейроны гипоталамуса воспринимают, обрабатывают и реагируют на сигналы от жировой ткани (лептин), поджелудочной железы (инсулин), и прочие гормональные стимулы (грелин, холецистокинин, панкреатический полипептид и др.). Гипоталамус управляет деятельностью эндокринной системы человека благодаря тому, что его нейроны способны выделять нейроэндокринные трансмиттеры, стимулирующие или угнетающие выработку гормонов гипофизом. Иными словами, гипоталамус, масса которого не превышает 5 % мозга, является центром регуляции эндокринных функций и поддержания гомеостаза всего организма.
Еще Дильман (Дильман В. М «Большие биологические часы») указывал на ведущую роль гипоталамуса в планомерном развитии метаболической дисфункции, приводящей к ожирению, сахарному диабету, сердечно-сосудистым, онкологическим заболеваням и старению. Согласно сформированной Дильманом теории гиперадаптоза чувствительность рецепторов гипоталамуса к сигналам, поступающим от тканей организма (лептин, инсулин и др.) постепенно планомерно снижается с возрастом. Для того, чтобы вызывать его «ответ» нужно все больше и больше того или иного гормона, — больше инсулина, больше лептина. Развивается инсулин- и лептинрезистентность, метаболические заболевания, приводящие к старению и смерти.
В зависимости от выполняемых функций группы нейронов объединяют в ядра гипоталамуса. Одно из них – аркуатное (дугообразное) ядро является ключевым регулятором пищевого поведения и обмена веществ. В нем могут образовываться орексигенные нейропептиды (стимулируют аппетит) и анорексигенные (подавляют аппетит), относящиеся, соответственно к AgRP и POMC нейронам. Периферические сигналы (инсулин, грелин, лептин и др) влияют на экспрессию пептидов, стимулирующих либо подавляющих аппетит, что обеспечивает слаженность центральной регуляции (рис.5).
Так кто и как регулирует чувствительность нейронов гипоталамуса?
В AgRP нейронах (hunger-promoting AgRP neurons), которые стимулируют аппетит и регулируют набор массы, голодание приводит к делению митохондрий, а high-fat feeding – к слиянию. То есть ответ митохондрий отличается от такового в большинстве других клеток.
Слияние МХ в этих нейронах регулирует электрическую активность в ответ на высокожировую диету, стимулируя выработку орексигенного пептида (AgRP пептида) оно необходимо для набора веса и отложения жира при избытке питательных веществ. Делеции Mfn1 и Mfn2 в этих нейронах приводили к меньшему набору веса у крыс за счет снижения уровня циркулирующего лептина.
РОМС нейроны (подавляют аппетит) имеют противоположную функцию, и динамика митохондрий в ответ на поступление питательных веществ у них иная. Снижение экспрессии митофузинов в этих нейронах приводит к нарушению связи митохондрий с ЭПС, а в результате – гиперфагия, лептинрезистентность и ожирение. При этом возрастало употребление пищи, а энергозатраты снижались.
Таким образом, ответ организма на высокожировую диету зависит от паттернов динамики митохондрий в нейронах гипоталамуса. Ремоделирование митохондрий в нейронах обеспечивает их ответ на поступление в организм питательных веществ, стимулирует выработку нейропептидов, которые будут либо стимулировать либо подавлять аппетит, влияя на метаболизм на уровне организма (Рис.6).
В ответ на экзогенные стимулы Mfns вовлечены в трансдукцию метаболического сигналинга в разных органах, что обеспечивает поддержание гомеостаза энергии всего организма. В частности, в ответ на потребление пищи, изменения температуры, стресс или физические упражнения, бурая жировая ткань, мозг, сердце или скелетные мышцы адаптируют свой метаболизм для контроля питания, веса тела, сократительных функций, антиоксидантного ответа или чувствительности к инсулину.
Как повлиять на динамику митохондрий?
1. Питание и физические упражнения
Calorie restriction (fed/fasting cycle) стимулирует биоэнргетическую адаптацию, обеспечивая работу механизмов качества митохондрий.
2. Здоровые мембраны: стеариновая кислота, кардиолипин, фосфатидная кислота
От «здоровья» мембран митохондрий зависят все ключевые процессы, — аутофагия, митофагия, апоптоз, связь митохондрий с эндоплазматической сетью, динамика митохондрий. Мембраны клеточных органелл состоят из липидов и из белков. Ремоделирование этих мембран контролируется взаимодействиями между специфическими липидами и белками.
Кардиолипин (СL) стимулирует деление митохондрий и слияние внутренних мембран.
Кардиолипин необходим для работы комплекса IV (цитрохром С оксидазы) электронтранспортной цепи. Кардиолипин находится практически исключительно во внутренней мембране митохондрий. С возрастом происходит снижение количества кардиолипина. Есть теория, что потеря функции кардиолипина связана с заменой насыщенных жирных кислот в его молекуле полиненасыщенными жирными кислотами. Для решения этого вопроса необходимо вводить в рацион насыщенные жиры, богатые, в первую очередь, стеариновой жирной кислотой.
Фосфатидная кислота (РА) ингибирует митохондриальное деление и стимулирует слияние внешних мембран (рис.7).
Во внешней мембране (ОМ) РА стимулирует митофузин-опосредованное (Mfn) слияние. Во внутренней мембране (IM) CL стимулирует Opa1-опосредованное слияние. Сокращения: ER — эндоплазматический ретикулум; MitoPLD,- митохондрия-локализованная фосфолипаза D.
3. Регуляция экспрессии митофузинов (белков, отвечающих за динамику митохондрий)
Все, о чем мы говорили выше (сalorie restriction, стеариновая кислота, фосфолипиды) действуют, влияя на экспрессию митофузинов.
Помимо этого, есть ряд препаратов, которые опосредованно могут влиять на динамику митохондрий. К ним можно отнести использование метформина.
Генная терапия митохондрий
Нарушение динамики митохондрий может быть связано с нарушением экспрессии белков, отвечающих за слияние и деление митохондрий. Помимо этого, нарушение функции этих белков может быть связано (и это и происходит чаще всего) с их мутациями. Тут есть два подхода к рассмотрению причинно-следственных взаимодействий нарушения функции митохондрий.
Перенос митохондрий
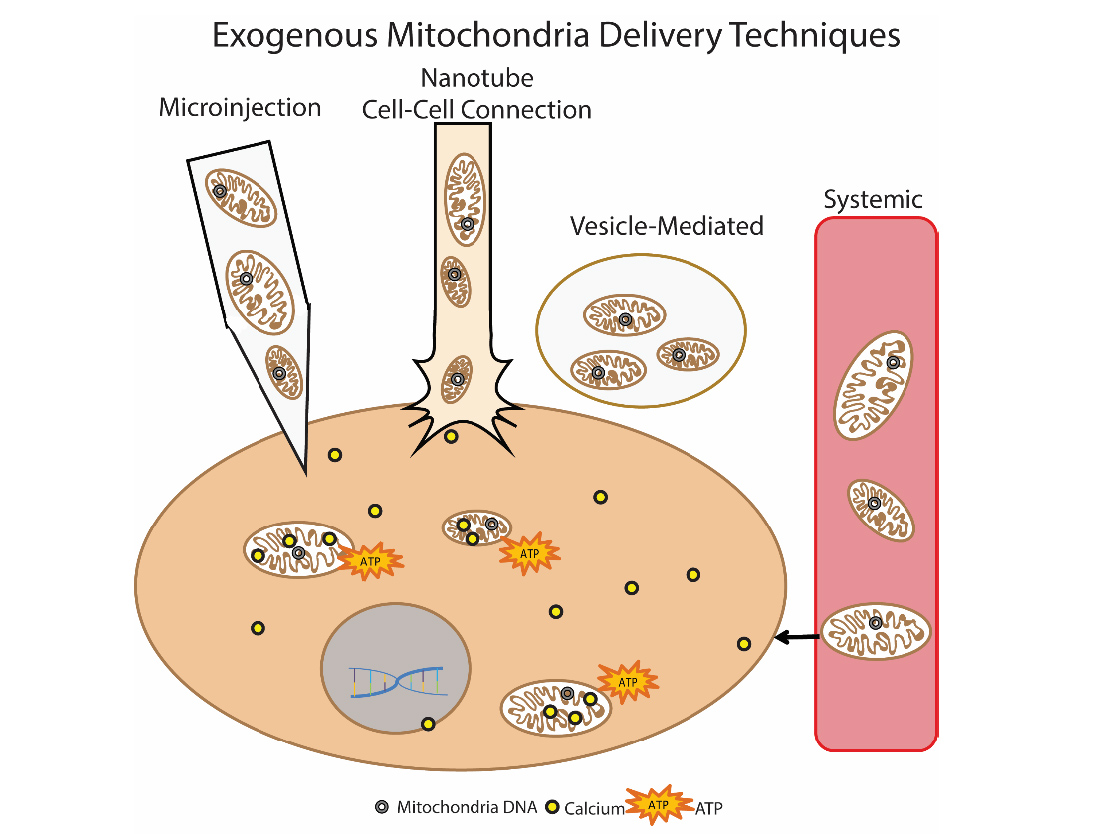
Рис.9 Способы доставки экзогенных митохондрий в клетку
Автор Ольга Борисова
1. Kauppila, Timo ES, Johanna HK Kauppila, and Nils-Göran Larsson. «Mammalian mitochondria and aging: an update.» Cell metabolism 25.1 (2017): 57-71.
www.sciencedirect.com/science/article/pii/S1550413116305022
2. Schrepfer, Emilie, and Luca Scorrano. «Mitofusins, from mitochondria to metabolism.» Molecular cell 61.5 (2016): 683-694.
www.sciencedirect.com/science/article/pii/S1097276516001337#fig1
3. Marc Liesa, Orian Shirihai “Mitochondrial Dynamics in the Regulation of Nutrient Utilization and Energy Expenditure” Cell methabolism (2013): 491-506
www.sciencedirect.com/science/article/pii/S1550413113001046#fig3
4. Ramos, Eduardo Silva, Nils-Göran Larsson, and Arnaud Mourier. «Bioenergetic roles of mitochondrial fusion.» Biochimica et Biophysica Acta (BBA)-Bioenergetics 1857.8 (2016): 1277-1283.
www.sciencedirect.com/science/article/pii/S0005272816300858
5. Cunarro, Juan, et al. «Hypothalamic mitochondrial dysfunction as a target in obesity and metabolic disease.» Frontiers in endocrinology 9 (2018): 283.
www.frontiersin.org/articles/10.3389/fendo.2018.00283/full
6. Marcelo O.Dietrich et al. «Mitochondrial Dynamics Controlled by Mitofusins Regulate Agrp Neuronal Activity and Diet-Induced Obesity”.
www.sciencedirect.com/science/article/pii/S0092867413010957#figs2
7. Steculorum, Sophie M., and Jens C. Brüning. „Sweet mitochondrial dynamics in VMH neurons.“ Cell metabolism 23.4 (2016): 577-579.
www.sciencedirect.com/science/article/pii/S1550413116301176
8. Senyilmaz-Tiebe, Deniz, et al. „Dietary stearic acid regulates mitochondria in vivo in humans.“ Nature communications 9.1 (2018): 3129.
www.nature.com/articles/s41467-018-05614-6
9. Kameoka, Shoichiro, et al. „Phosphatidic Acid and Cardiolipin Coordinate Mitochondrial Dynamics.“ Trends in cell biology (2017).
www.sciencedirect.com/science/article/pii/S0962892417301587
10. raypeatforum.com/community/threads/mitolipin-liquid-saturated-phosphatidylcholine-pc-mix.10398
11. Miret-Casals, Laia, et al. „Identification of new activators of mitochondrial fusion reveals a link between mitochondrial morphology and pyrimidine metabolism.“ Cell chemical biology25.3 (2018): 268-278.
12. Kauppila, Timo ES, Johanna HK Kauppila, and Nils-Göran Larsson. „Mammalian mitochondria and aging: an update.“ Cell metabolism 25.1 (2017): 57-71.
13. Gammage et al. “Genome editing in mitochondria corrects a pathogenic mtDNA mutation in vivo” Nature medicine, 2017
www.nature.com/articles/s41591-018-0165-9
14. Emani, Sitaram M., et al. „Autologous mitochondrial transplantation for dysfunction after ischemia-reperfusion injury.“ The Journal of thoracic and cardiovascular surgery 154.1 (2017): 286-289.
www.jtcvs.org/article/S0022-5223(17)30258-1/fulltext
15. McCully, James D., et al. „Mitochondrial transplantation: From animal models to clinical use in humans.“ Mitochondrion 34 (2017): 127-134.
www.sciencedirect.com/science/article/pii/S1567724917300053
Много митохондрий не бывает (вместо вывода)
Митохондрии — наш верный спутник и помощник в повышении выносливости и спортивном долголетии. Используя нехитрые принципы тренировок, мы можем влиять как на количество, так и на качество работы наших энергетических станций. Однако самым важным аспектом в погоне за митохондрией является ежедневное наблюдение за своим состоянием, постепенное повышение как объема, так и интенсивности тренировок, а также соблюдение баланса нагрузки и качественного восстановления. Ваши мышцы и митохондрии скажут вам спасибо новым личным рекордом!
- Granata C, Jamnick NA, Bishop DJ. Principles of Exercise Prescription, and How They Influence Exercise-Induced Changes of Transcription Factors and Other Regulators of Mitochondrial Biogenesis. Sports Med. 2018 Jul;48(7):1541-1559.
- Heo JW, No MH, Park DH, Kang JH, Seo DY, Han J, Neufer PD, Kwak HB. Effects of exercise on obesity-induced mitochondrial dysfunction in skeletal muscle. Korean J Physiol Pharmacol. 2017 Nov;21(6):567-577.








