- Эффект Варбурга
- Чем занимаются митохондрии?
- Куда пропадают «плохие» митохондрии?
- Как митохондрии сливаются?
- Образование атф в клетке. Хемиосмотическая гипотеза Митчела.
- Митохондрии.
- Митохондрии — энергетические станции
- Жирные кислоты, церамиды и повреждения нейронов
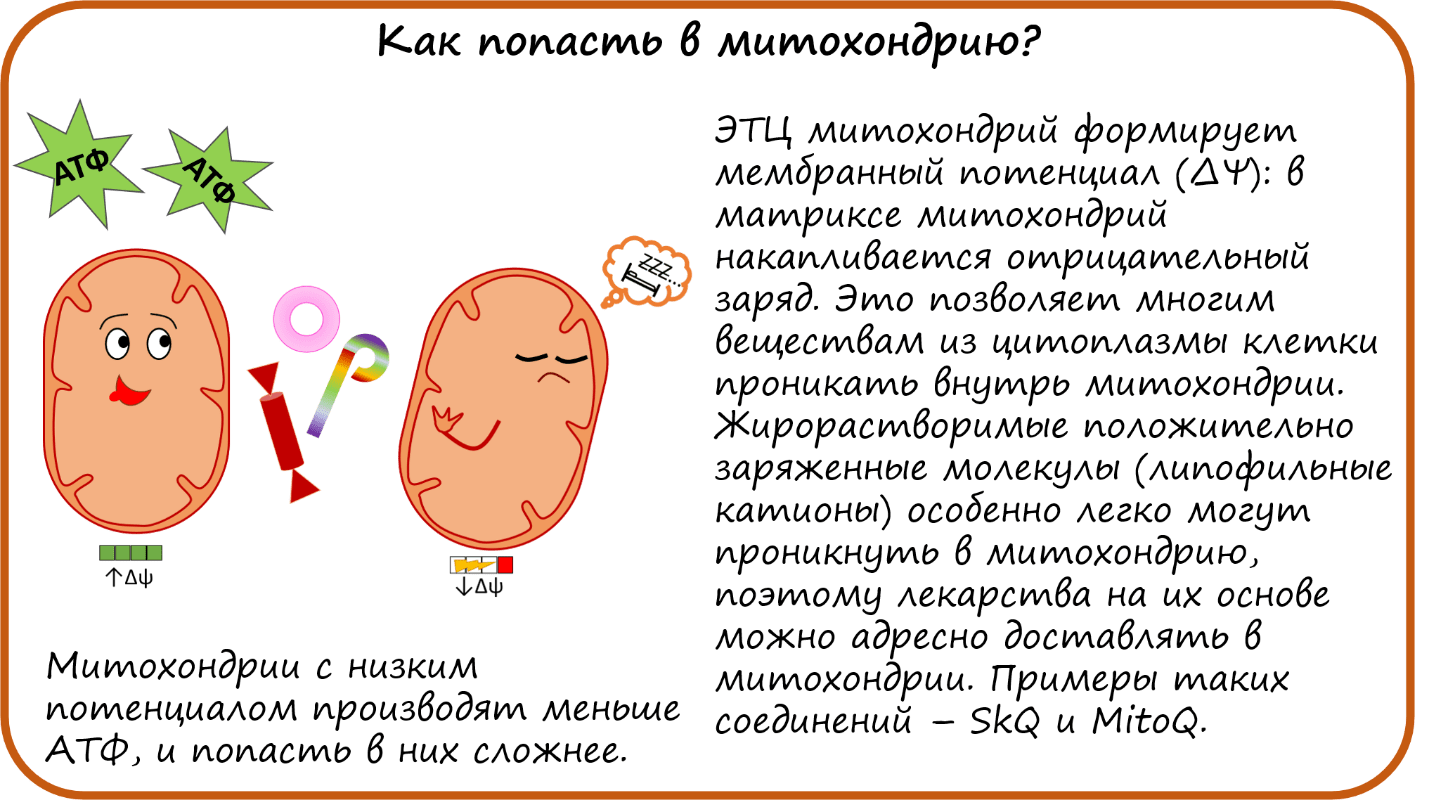
- Как попасть в митохондрию?
- Энергетический обмен, митохондрии
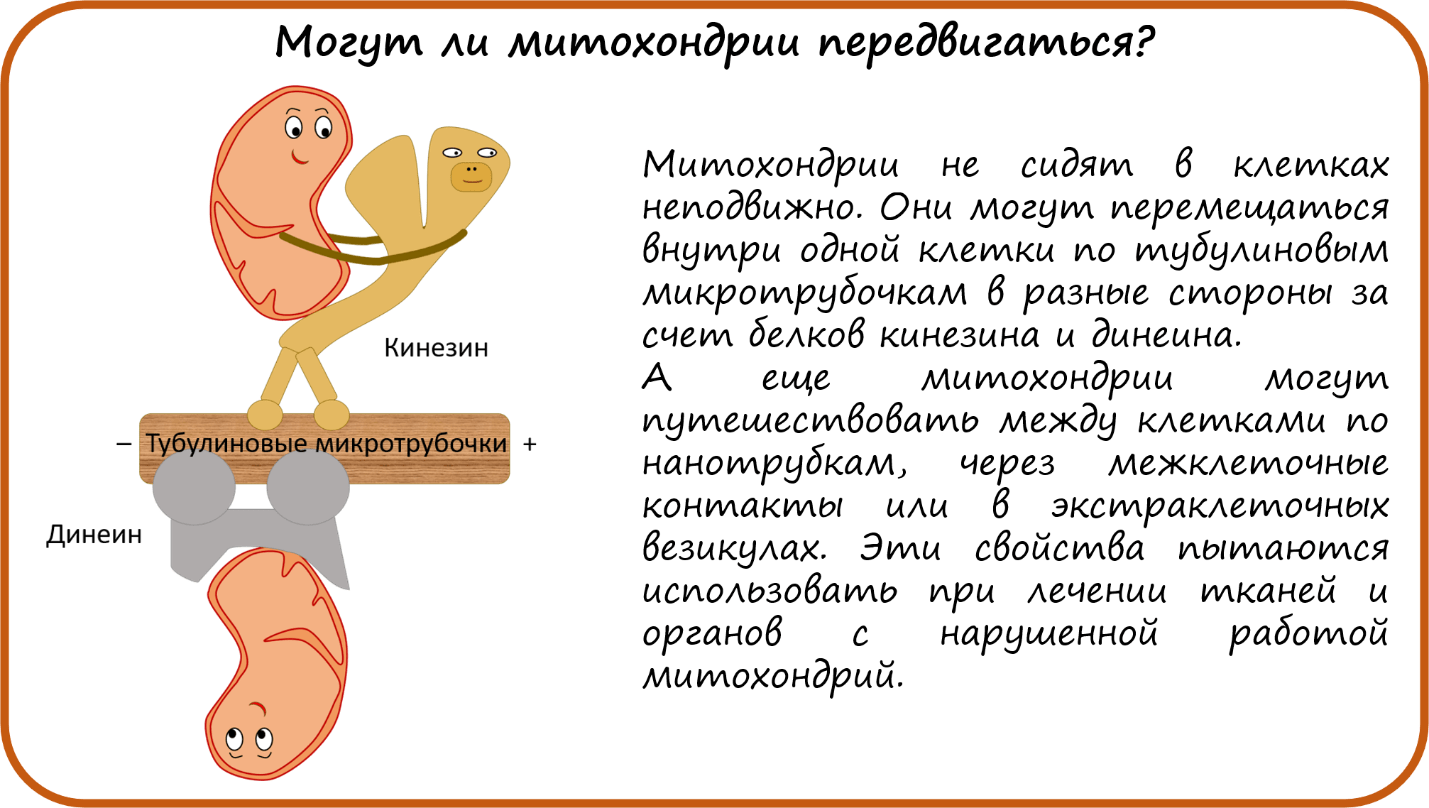
- Могут ли митохондрии передвигаться?
Эффект Варбурга
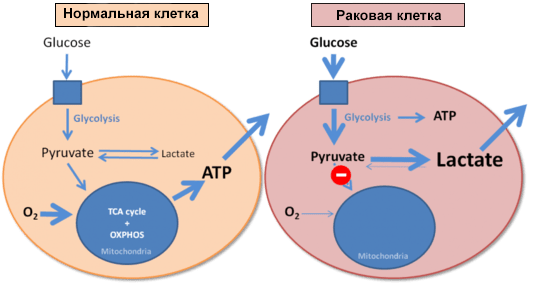
Рисунок 5. Энергообеспечение нормальной и раковой клеток. Синим квадратом обозначена поступающая в клетку глюкоза.
Таким образом, изменения в метаболизме глюкозы и появление дефектных белков и внутриклеточных агрегатов могут говорить о начале развития патологии. Своевременное выявление подобных внутриклеточных процессов может сыграть решающую роль в предупреждении и терапии самых распространенных нейродегенеративных и онкологических заболеваний. А для того чтобы это было возможным, необходимо изучать фундаментальные аспекты патологий, связанные с работой митохондрий и энергетическим обменом. Сегодня уже разработаны системы, позволяющие заглянуть «вглубь» этих заболеваний и даже провести диагностику на самой ранней стадии их развития. Подробнее об этих системах, принципах их действия и исследованиях с их использованием расскажут следующие статьи спецпроекта.
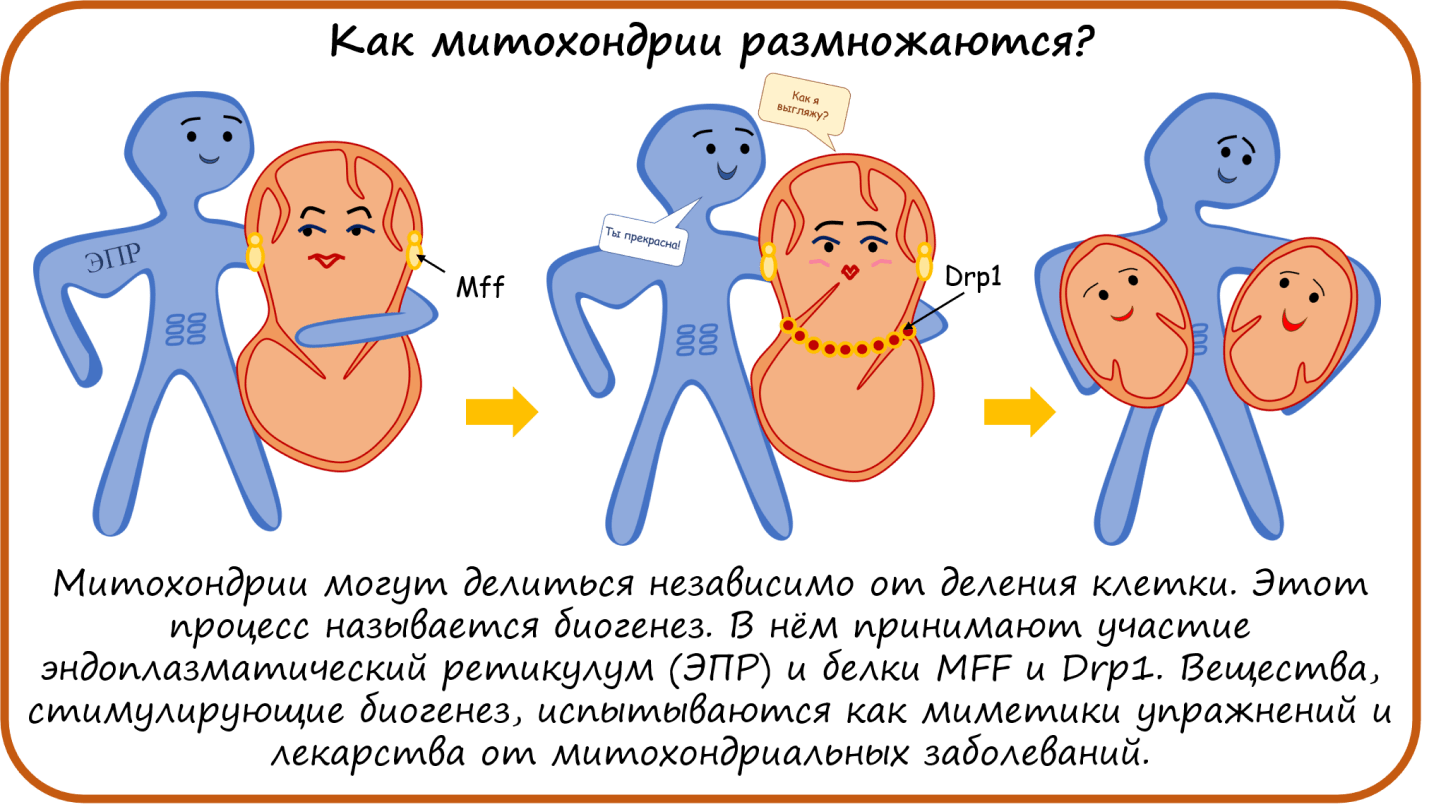
Чем занимаются митохондрии?
Большинство митохондриальных генов в процессе эволюции переместилось в клеточную ДНК, и только небольшая часть осталась в митохондриальном геноме.

Рисунок 8. Полет фантазии на тему происхождения митохондрий по мотивам «Рождения Венеры» Сандро Боттичелли.
Куда пропадают «плохие» митохондрии?
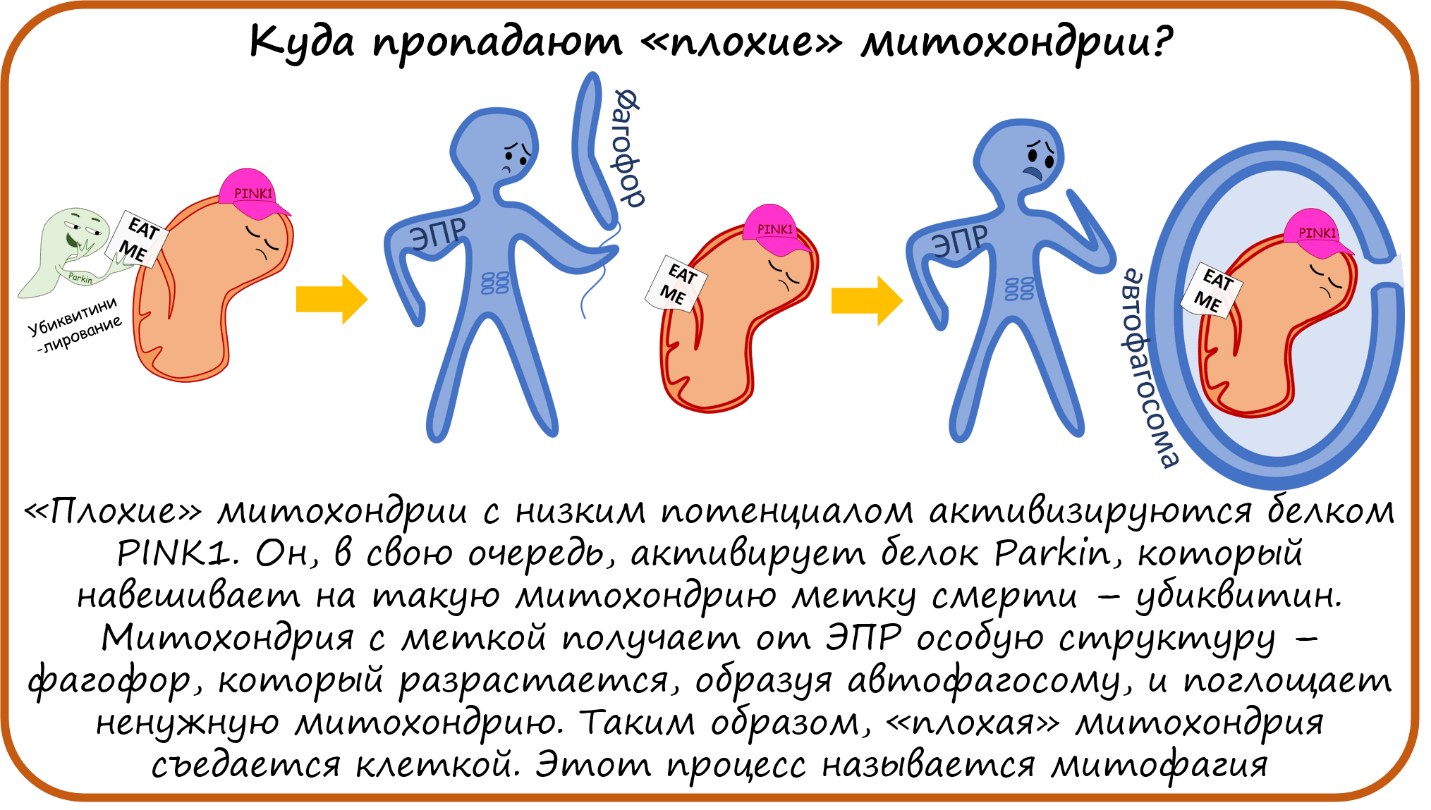
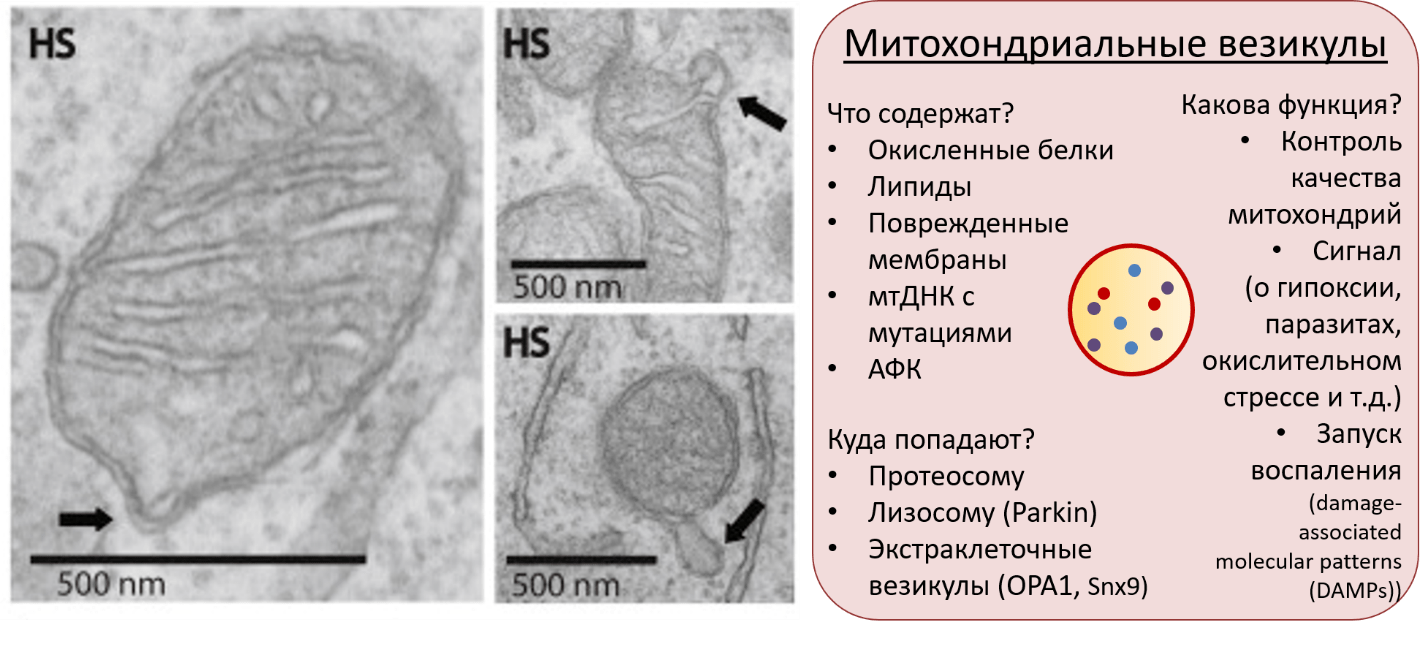
Рисунок 9. Слева — просвечивающие электронные микрофотографии митохондриальных везикул (mitochondria-derived vesicle, MDV). Справа — основные свойства MDV.
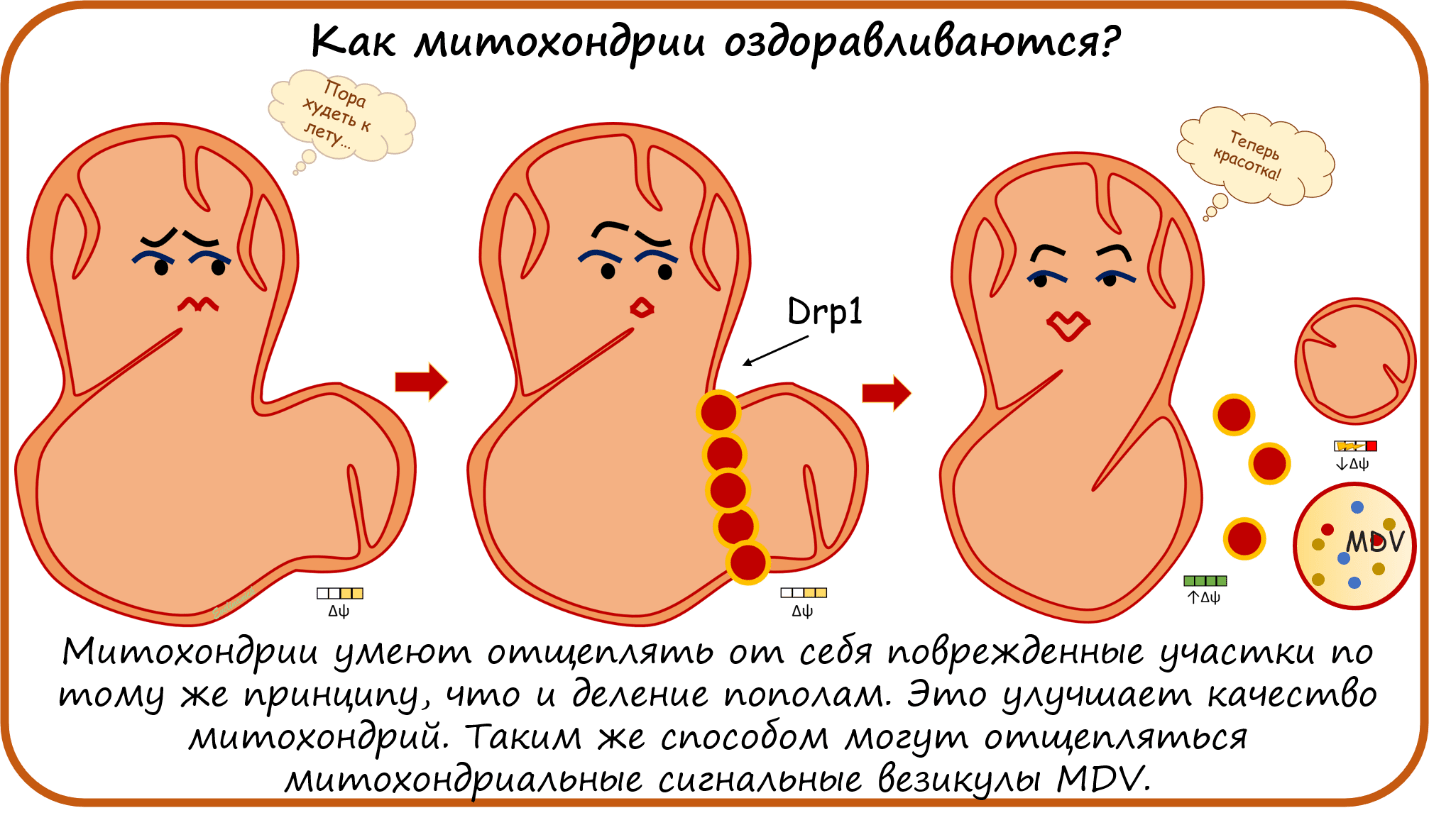
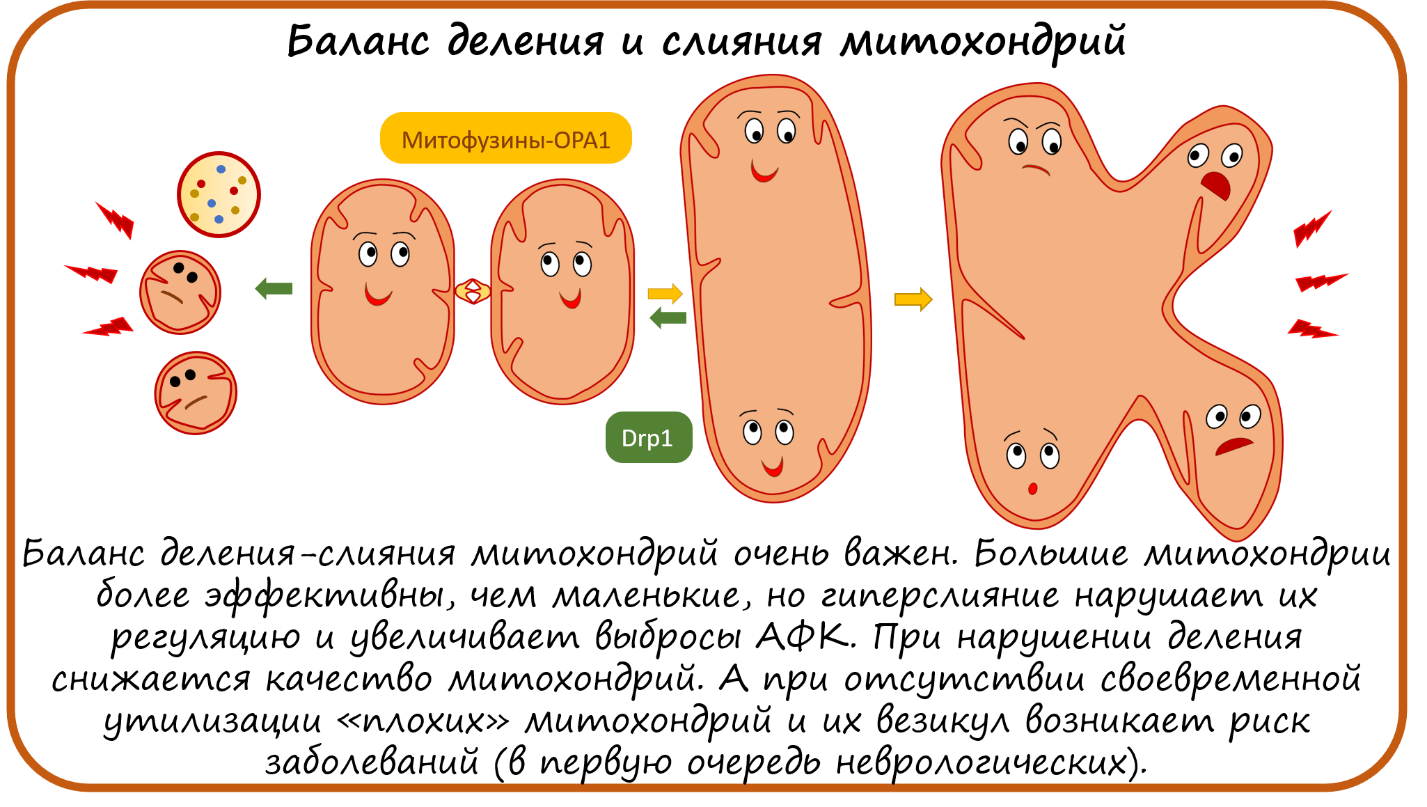
Как митохондрии сливаются?
Образование атф в клетке. Хемиосмотическая гипотеза Митчела.
См. 31 вопрос
Для образования АТФ ферментная система
АТФ-синтетаза использует разницу
электрохимических потенциалов и
концентрации ионов водорода на разных
сторонах мембраны, перераспределяя
поток водорода: с внешней мембраны
переносит ионы водорода на внутреннюю.
Во время перенесения электронов от НАДН
к кислороду выделяется энергия,
необходимая для синтеза трех молекул
АТФ.
Соседние файлы в предмете Биология
Митохондрии.
Открыл в 1848 году,
Альтман.
Есть почти у всех
эукариотов. Это подвижные органоиды,
могут менять свою морфологию, объединяться,
разъединяться с помощью микротрубочек.
Различные по форме.
Период жизни
митохондрий короток. У человека они
живут 9 суток. Более 10 суток митохондрии
не живут, т.е., высокая степень обновления.
Основная функция
митохондрий – синтез
АТФ, дающий
энергию для всех жизненных процессов.
Митохондрии встречаются практически
у всех эукариотических клеток, кроме
двух видов паразитических амеб.
Митохондрии являются подвижными
пластичными органоидами, они могут
объединяться в гигантские структуры и
наоборот – разрушаться. Совокупность
всех митохондрий в клетке – хондриом.
Размеры варьируют от 1 до 10 мкм. Форма
чрезвычайно разнообразна. Но несмотря
на разнообразие форм и размеров, для
всех митохондрий характерен единый тип
строения. Митохондрия состоит из двух
мембран, наружной и внутренней, меж
которыми находится межмембранное
пространство, которое по сути является
протонным резервуаром. Внутри –
митохондриальный
матрикс.
Наружная мембрана
характеризуется большим количеством
транспортных белков. Эти белки имеют
специфическое название порины.
Они образуют широкие гидрофильные
каналы в бислое липидов, которые
пропускают молекулы с молекулярной
массой до 10000 Дальтон. На наружной
мембране имеются ферменты, которые
превращают липиды в реакционноспособные
соединения. Белков менее 20%. Из физических
свойств можно отметить, что наружная
мембрана может только необратимо
растягиваться.
Внутренняя мембрана
легко сморщивается и растягивается.
Она образует многочисленные складки,
которые называются кристы. Площадь
внутренней мембраны почти в
пять-семь раз больше,
чем наружной. Кристы бывают двух типов
– пластинчатые
в клетках многоклеточных животных и
растений; трубчатые
в тканях синтезирующих ферменты. Кристы
не статистические образования. Расположены
параллельно или перпендикулярно длинной
оси митохондрий.
Степень развития
крист, их количество определяется
функциональной значимостью клетки. На
внутренней мембране очень низок уровень
холестерина. Много особого фосфолипида
кардиолипида. Благодаря этому мембрана
имеет малую
проницаемость.
При суммарном подсчете и вычислении
соотношения белков и липидов получим,
что белков 75%, а липидов 25%.
- Грибовидные тельца
с АТФ-синтетазой; - Специфические
транспортные белки, регулирующие
перенос метаболитов в матрикс митохондрий
и из матрикса.
Межмембранное
пространство или протонный резервуар.
По химическому составу почти идентичен
цитозолю. Содержится только несколько
ферментов для обеспечения реакции
фосфорилирования.
Матрикс –
высококонцентрированная смесь, более
чем из ста компонентов, большинство из
которых – это ферменты цикла Кребса
(карбоновых кислот). Здесь же располагаются
кольцевые молекулы, митохондриальная
ДНК, тРНК, иРНК и митохондриальные
рибосомы с константой седиментации от
55 до 75S
Белки цепи
переноски электронов.
Это крупные ферментные комплексы, по
которым электроны опускаются на все
более низкие энергетические уровни.
Конечным акцептором является молекулярный
кислород. В цепи выделяют электрон-собирающие
и электрон-распределяющие участки и
последовательные ряды ферментов, с
которыми взаимодействуют электроны,
можно разделить на три главных
ферментативных комплекса:
- НАДН+-дегидрогеназный
комплекс. Состоит из двенадцати
полипептидных цепочек. Главные из этих
компонентов является НАДН+
и убихинон (ко Q). НАДН+-дегидрогеназа
первая принимает 2 протона и 2 электрона.
Убихинон –
небольшой переходный переносчик,
который тоже принимает и протоны и
электроны. Переносит протоны через
мембрану на наружную поверхность
сопрягающей мембраны. - Комплексу B=С
Этот комплекс состоит из 8 полипептидных
цепей. Содержит два цитохрома (В и С),
которые передают только электроны, а
протоны сбрасываются в межмембранное
пространство.
При этом, цитохром
С, принимающий электроны, передает их
на 3 комплекс.
Особую роль играют
Fe содержащие полипептиды. Они различаются
между собой в степени сродства к
электронам, которое выражается через
окислительно-восстановительный потенциал
молекулы. Чем выше этот потенциал, тем
больше сродство окисленной молекулы к
электрону. Электроны переходят по цепи
переноса. Их коферменты восстанавливаются
и окисляются. Цитохромидаза передает
электрон с комплекса цитохрома на
молекулярный кислород. Кислород
активируется и связывается с электронами.
Это важная реакция, в ней кислород
приобретает отрицательный заряд,
благодаря чему водород соединяется с
ним, и образуются вода.
Электроны
перемещаются в толще внутренней мембраны,
при этом через внутреннюю мембрану они
не проходят и остаются на внутренней
стороне мембраны. Протоны обратно не
возвращаются. Они остаются на внешнем
мембранном пространстве. На каждую
исходную молекулы C6H12O6
64 протона. В результате работы дыхательной
цепи на мембранах создается разных
электрических потенциалов. Внутренняя
сторона мембраны заряжается отрицательно
за счет скопления на ней электронов, а
наружная сторона внутренней мембраны
заряжается положительно.
Кроме того, поток
протонов создает между двумя сторонами
внутренней мембраны разность значения
рН. Таким образом, мы имеем кроме
мембранного потенциала еще и градиент
рН. Вместе они составляют электрохимический
протонный градиент. Величина
электрохимического протонного градиента,
который стимулирует синтез, равно 200
мВ. Заствляет ионы двигаться внутрь
матрикса. Заряд – источник протон-движущей
силы.
Грибовидное тело.
Белковый комплекс, который состоит из
двух основных частей: ножки (протон-движущий
канал) и головки (сопрягающего фактора).
Ножка находятся в толще внутренней
мембраны, имеет гидрофобную природу и
по сути является протон-проводящим
канал, по которому протоны из межмембранного
пространства возвращаются в матрикс
митохондрий
Головка тела
называется сопрягающий фактор. Здесь
располагается фермент АТФ-синтетаза,
который превращает энергию движения
протона в энергию органического синтеза,
синтезируя АТФ из молекулы АДФ и
неорганического фосфата (реакция
фосфорилирования).
АТФ занимает 15%
всех белков и образуется при прохождении
1-2 протонов.
Субстратами для
дыхания служат неорганические соединения.
Большинство клеток используют углеводы.
Вовлекаются в процесс расщепления
только после гидролиза до моносахаридов.
Крахмал гидрализуется в глюкозу. Гликоген
гидролизуется примерно до 30000 остатков
глюкоз. Ферментативное расщепление
этих запасных углеводов составляет
первый подготовительный этап
энергетического обмена. Вторым этапом
энергетического обмена является неполное
окисление глюкозы. Оно всегда
бескислородное. Всегда происходит
непосредственно в цитоплазме клетки и
называется гликолизом.
Гликолиз – неполное бескислородное
расщепление глюкозы или многоступенчатый
процесс по превращению углерода в 2
молекулы пировиноградной кислоты
(С3Н4О3).
В ходе гликолиза
выделяется большое количество энергии
(200 кДж на моль), 60% этой энергии рассеивается
в виде тепла, а 40% используется на синтез
АТФ. Кроме двух молекул пирувата,
образуются протоны, которые в цитоплазме
клетки запасаются в форме переносчика.
У животных преобладающим переносчиком
является НАДФ и соединяется с протоном.
Дальнейшая судьба
пирувата имеет три пути:
1) Характерный для
дрожжей и клеток растений при недостатке
кислорода происходит спиртовое брожение
и ПВК восстанавливается до этилового
спирта (С2Н5ОН).
2) В клетках животных
при недостатке кислорода. Накопление
в мышечных волокнах молочной кислоты.
Пируват восстанавливается до молочной
кислоты (С3Н6О3).
3) При наличии в
среде кислорода, продукты гликолиза
расщепляются до СО2
и Н2О
(полное окисление или клеточное дыхание).
Продукты гликолиза переходят для
дальнейшего расщепления в матрикс
митохондрий, где протекает третий этап
энергетического обмена – клеточное
дыхание. Пируват, одновременно с потоком
протонов, направляется внутрь митохондрий.
В матриксе молекулы пирувата взаимодействуют
с каталитическими белками и преобразуется
в молекулу ацетил-коА.
Только он
может вступить в цикл Кребса. Он
вовлекается в цикл трикарбоновых кислот,
который представляет собой цепь
последовательных реакций, в ходе которых
из одной молекулы ацетил-коА образуются
молекулы углекислого газа, 2 АТФ и 4 атома
водорода. Таким образом, в результате
бескислородного окисления и цикла
Кребса, одна молекула глюкозы расщепляется
до диоксида углерода, который легко
выходит из клетки через мембрану и
высвобождающееся при реакции энергия
расходуется в небольшом количестве на
синтез АТФ, а в основном запасается в
нагруженных электронами переносчиков.
Белки-переносчики транспортируют
протоны и электроны к внутренней мембране
митохондрий, где передают их на цепь
дыхательных ферментов.
Транспорт протонов
и электронов приводит к накоплению в
протонном резервуаре протонов. Наружная
поверхность внутренней мембраны заряжена
положительно. Электроны обеспечивают
отрицательный заряд внутренней стороны
мембраны. Когда разность потенциалов
= 200мВ, открывается канал в ножке
грибовидного тела, протоны проталкиваются
через ножку, отдавая энергию ферменты
АТФ-синтетазе, что обеспечивает реакцию
фосфорилирования.
Синтез АТФ сопряжен
с обратным потоком протонов в матрикс.
Протонный градиент
через внутреннюю мембрану митохондрий
дает примерно 24 кДЖ на моль переносимых
протонов. И процесс переноса электронов
(окисление) в мембранах связан с
образованием АТФ из АДФ (реакция
фосфорилирования) и поэтому весь
называется окислительное фосфорилирования.
Ведущую роль в
этих реакциях выполняет внутренняя
сопрягающая мембрана митохондрий. В
процессе окислительного фосфорилирования
перенос каждой пары электронов с
переносчика на молекулярный кислород
доставляет энергию примерно для
образования трех молекул АТФ. При
окислении одной молекулы глюкозы
образуется в реакциях третьего этапа
36 молекул АТФ. Две молекулы АТФ образуются
в бескислородном втором этапе обмена
и поэтому общий выход = 38 молекул АТФ на
одну полностью окисленную молекулу
глюкозы. 55% энергии запасается в виде
химических связей, 45% энергии рассеивается
в виде теплоты.
Сопряжение окисления
и фосфорилирование известно как
хемиосмотическая гипотеза Митчела.
В1978 году он был лауреатом нобелевской
премии за исследование процесса переноса
энергии в клетках и разработку
хемиосмотической теории. Эта теория
объясняет механизм преобразования
энергии в биологической мембране при
синтезе АТФ.
Обмен веществ
между цитоплазмой и матриксом
обеспечивается специальными транспортными
системами, локализованными во внутренней
мембране митохондрии и обеспечивающие
перенос веществ разными механизмами
активного транспорта.
1) По механизма
типа антипорт, когда два вещества
переносятся одновременно в противоположных
направлениях. Большая часть АТФ,
продуцированная митохондриями, выходит
в цитоплазму. Этот перенос осуществляется
АТФ-АДФтранслоказой
2) Симпорт или
сопряженный транспорт. Таким образом,
при участии специфического переносчика
осуществляется одновременный перенос
пирувата и ионов фосфата и протонов.
3) Унипорт. Облегченная
диффузия. Только одно вещество переносится
через мембрану в одном направлении
(ионы кальция внутрь матрикса). С помощью
транспортных белков.
Митохондрия –
полуавтономный органоид. Митохондрии
увеличиваются в количестве при делении
клеток (особенно в период G2),
при увеличении функциональной активности
и нагрузки клетки. Увеличение их
количества происходит путем роста и
деления материнских митохондрий. Делятся
митохондрии путем перетяжки, или
отпочковывания, или возникновения
дочерних митохондрий внутри материнских.
В матриксе
митохондрий содержится собственная
генетическая система, необходимая для
процессов воспроизведения. Это
митохондриальная ДНК, митохондриальные
рибосомы. Гистонов нет. Эти структуры
были обнаружены в 1963 году Нассом.
Митохондриальная ДНК имеет кольцевую
природу. Известно, что все митохондрии
содержат несколько копий своего генома.
От одной копии до десяти. Линейная длина
молекулы варьирует от 5 до 30 мкм. Из
нуклеотидных оснований преимущественно
гуанин и цитозин.
Рибосомы вариабельны,
с константой седиментации 55 – 75S. В 1981
году была расшифрована нуклеотидная
последовательность митохондриального
генома человека. Было показано, что в
митохондриях человека содержится 2 гена
рРНК, 22 гена тРНК и 13 генов, которые
кодируют белки. Репликация и транскрипция
происходят в матриксе митохондрий, и в
этих процессах преобладает контроль
со стороны ядерного генома. Делению или
репродукции митохондрий обязательно
предшествует репликация митохондриальной
ДНК. И этот процесс происходит независимо
от репликации ядерной ДНК. Но обычно
тогда, когда уже ядерная ДНК вся
реплицировалась.
Происхождение и
эволюцию митохондрий объясняют с позиции
эндосимбиотической
гипотезы. И
эта же самая гипотеза представляет
современные митохондрии прямыми
потомками бактериального симбионта.
Это особая группа фотосинтезирующих
бактерий, которые утратили, внедрившись
в организм хозяина, способность к
фотосинтезу, но сохранили дыхательную
функцию. Эти пурпурные бактерии,
внедрившись в другую эукариотическую
клетку, укоренились к ней.
Последние наблюдения
цитологов после расшифровки генома
показали, что митохондрии эволюционировали
вместе со всеми эукариотами от одного
общего предка (коэволюция – совместная
эволюция). Эволюционно, митохондриальный
и ядерные
компоненты
эукариот возникли одновременно.
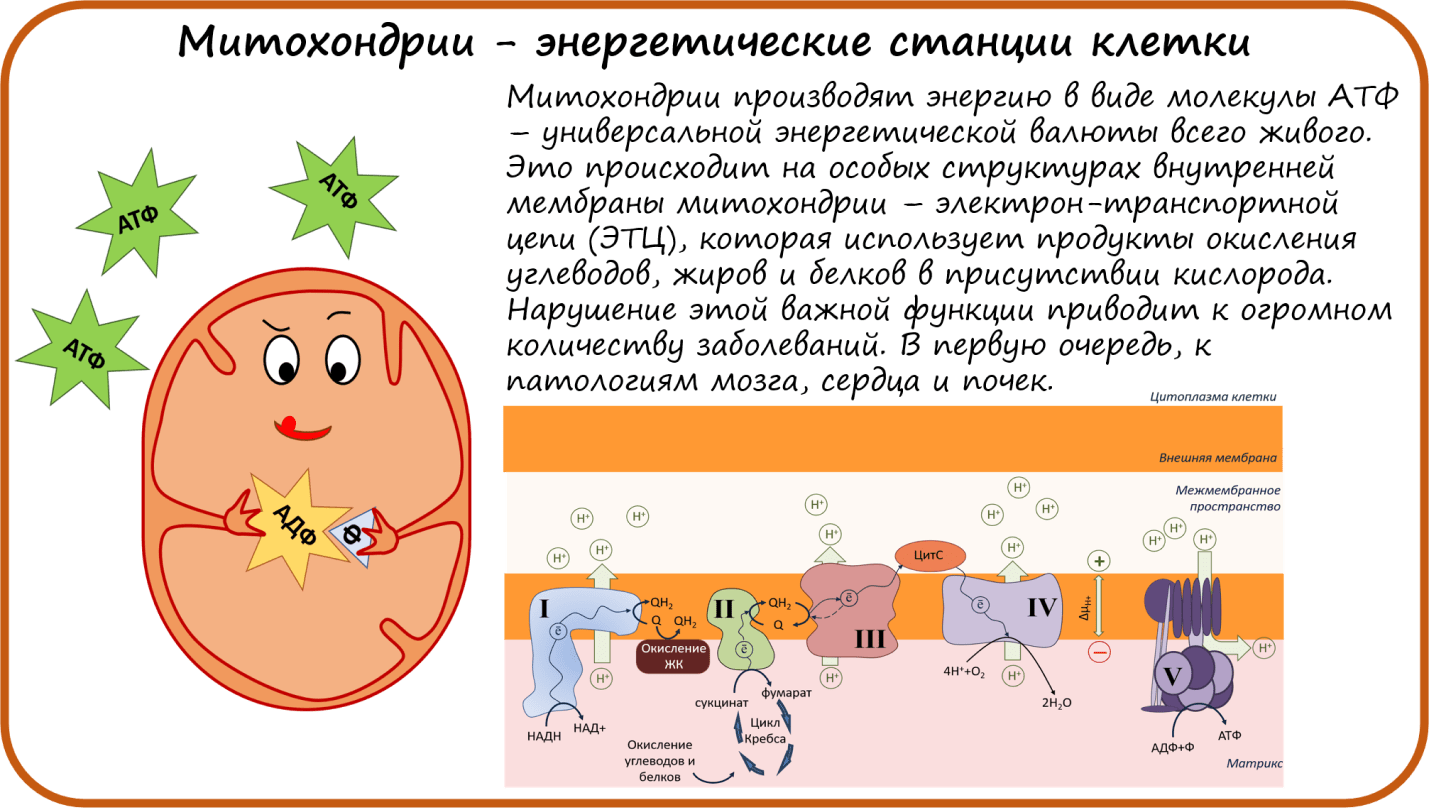
Митохондрии — энергетические станции
Все мы дышим и едим. Оба этих неотъемлемых атрибута нашей жизнедеятельности обусловлены наличием в наших клетках микроскопических органелл — митохондрий . Потребляя белки, жиры и углеводы, мы снабжаем наши митохондрии необходимыми субстратами для производства молекул АТФ — универсальной энергетической валюты всех живых клеток. За счет энергии АТФ в клетках нашего организма происходят практически все биохимические процессы, необходимые для жизнедеятельности, движения и мышления. Кислород является обязательным условием для работы митохондрий, без него уже в течение нескольких минут клетки начинают погибать.
Организмы, не имеющие митохондрий, могут вовсе не нуждаться в питании органикой и дыхании кислородом. Например, некоторые бактерии-хемосинтетики живут в бескислородной среде и получают всю необходимую энергию за счет энергии химических связей (сероводорода, сульфидов, железа и т.д.), а в качестве источника углерода эти организмы используют не органические соединения, а углекислый газ.

Рисунок 1. (а), (б) — просвечивающая электронная микрофотография среза сердца крысы. (б), (в) — желтым цветом обведены контуры мембран митохондрии, стрелками обозначены внутренние структуры: матрикс, межмембранное пространство (ММП) и кристы
фотография автора на просвечивающем электронном микроскопе JEM-1011 в ЦКП МГУ
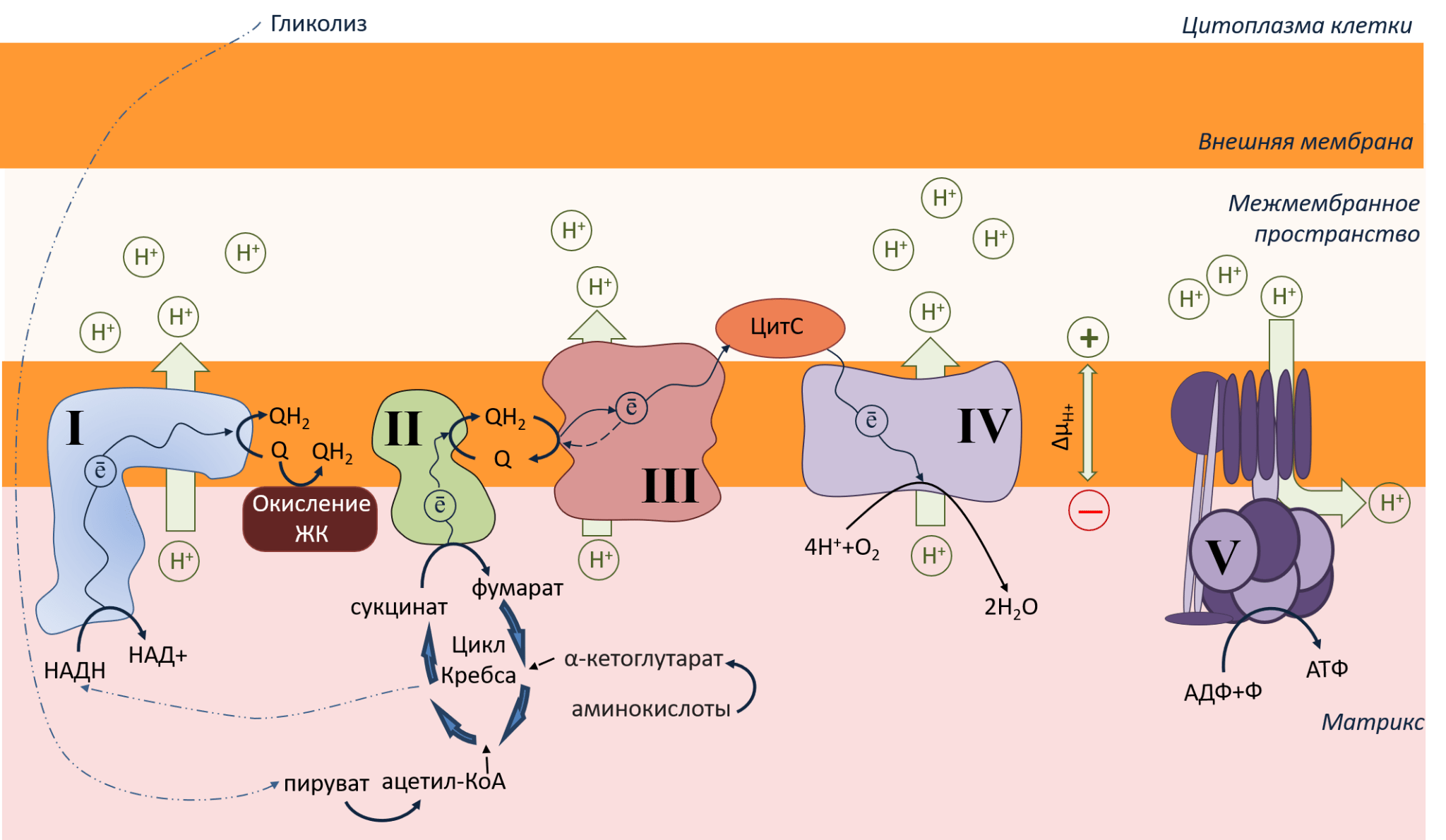
Рисунок 2. Схематичное изображение небольшого участка митохондрии: внутренняя, внешняя мембрана, межмембранное пространство. Темно-синими стрелками показан путь электрона вдоль мембраны. Зелеными стрелками показано движение протонов через мембрану. Описание в тексте.
Рассмотрим рисунок 2. На внутренней мембране расположены крупные белковые комплексы. Это электрон-транспортная цепь (ЭТЦ), или дыхательная цепь митохондрий. Почему она так называется? По этой ЭТЦ от I и II до IV комплекса бегут электроны, как ток по проводам (путь электронов — ē — показан темно-синими стрелками). Внутри комплексов ЭТЦ находятся особые молекулы — кофакторы (железосерные кластеры, флавины, цитохромы), расположенные в таком порядке, чтобы электроны легко перебегали по ним в нужном направлении .
Строго говоря, направление движение электронов по ЭТЦ обеспечивается редокс-потенциалами (или окислительно-восстановительными потенциалами) кофакторов комплексов ЭТЦ: электроны перемещаются от молекул с донорными свойствами (с низким редокс-потенциалом), то есть легко отдающим электрон, к молекулам с акцепторными свойствами (с высоким редокс-потенциалом), легко принимающим электрон. При перемещении электрона донор окисляется, а акцептор восстанавливается. Наиболее подробно этот процесс описан в классических учебниках по биохимии Ленинджера (глава 19) и по биоэнергетике Николлса (глава 3) или Скулачева с соавт. (глава 4).
Откуда ЭТЦ берет электроны? В цитоплазме клетки происходит гликолиз — окисление глюкозы до пирувата, который попадает в матрикс митохондрий, где участвует в цикле Кребса . В результате этого процесса образуются две важные молекулы: НАДН и сукцинат. Эти молекулы и служат донорами электронов в ЭТЦ. Они отдают свои электроны комплексу I и комплексу II, окисляясь до НАД+ и фумарата. С этих комплексов электроны поступают на молекулы убихинонов (коферменты Q) — единственных подвижных жирорастворимых переносчиков электронов в ЭТЦ. Также коферменты Q получают электроны от окисления жирных кислот (ЖК). Убихиноны с электронами (то есть в восстановленном состоянии) называются убихинолы. Они доплывают до комплекса III, передавая электрон на цитохромы типа В.
Не только углеводы являются поставщиками субстратов для цикла Кребса. Еще это делают белки в результате так называемых анаплеротических (то есть дополнительных) реакций.
Далее путь электронов раздваивается: один электрон возвращается на хинон, а второй — поступает на цитохром С (ЦитС) — единственный мобильный водорастворимый переносчик электронов, который плавает в межмембранном пространстве и «довозит» электрон до IV комплекса. Это финальная точка ЭТЦ. Электроны, добежавшие до конца, выполнили свою задачу и уже больше никому не нужны. Они утилизируются с помощью кислорода (О2). Кислород работает чем-то вроде мусорной корзины для электронов, забирая их из ЭТЦ, и, соединяясь с протонами, превращается в воду (Н2О).
Жирные кислоты, церамиды и повреждения нейронов
Как выяснилось, избыток жирных кислот и дисфункция митохондрий напрямую связаны с возникновением возрастных нейродегенеративных патологий. Надо сказать, что клетки нервной системы — самые уязвимые для возрастного окислительного стресса и снижения синтеза АТФ. Такая исключительная чувствительность нейронов к дефициту энергии и повышению генерации АФК объясняется несколькими причинами.
Во-первых, нервная ткань в силу своей физиологии нуждается в наибольшем потреблении кислорода. Вследствие этого в митохондриях нейронов происходит интенсивный окислительный метаболизм, который и становится основной причиной повышенной генерации АФК.
Как попасть в митохондрию?
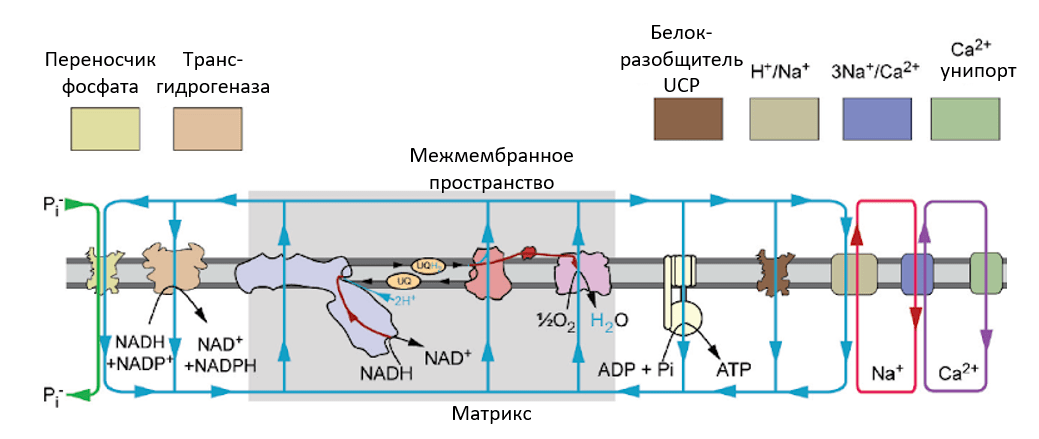
Рисунок 3. «Потребители» потенциала митохондрий: перенос ионов (фосфата, кальция и натрия) между матриксом и межмембранным пространством (а затем и цитоплазмой клеток) обеспечивается рядом белковых транспортеров за счет энергии мембранного потенциала. Кроме этого, мембранный потенциал необходим для транспорта образовавшихся в матриксе митохондрий молекул АТФ в цитоплазму клеток, для создания восстановительного эквивалента НАДФН из НАДН и для многих других процессов.
Энергетический обмен, митохондрии
Каждая клетка –
сложная высокоупорядоченная система
и содержимое клетки находится в состоянии
непрерывного активного метаболизма.
Реакции в клетке
подразделяют на две группы:
1) Реакции синтеза
крупных молекулярных структур, которые
протекают с затратой энергии, называются
реакциями синтеза, ассимиляцией или
анаболизмом.
2) Реакции распада
крупных молекул на более мелкие и
простые, протекающие обычно с высвобождением
энергии. Реакции диссимиляции или
катаболизма.
Реакции ассимиляции
формируют так называемый пластический
тип метаболизма. А реакции диссимиляции
– это реакции энергетического обмена.
Все реакции
пластического и энергетического обмена
можно назвать метаболизмом.
Поступающие в
клетку вещества служат строительным
материалом для биосинтеза клеточных
структур и компонентов клетки, а
во-вторых, эти же вещества являются
источником химической энергии.
У всех эукариотических
клеток можно выделить три типа органоидов
энергетического обмена. В растительных
клетках это тилакоидные мембраны
пластиды,
в животных – внутренние мембраны
митохондрий,
а у аэробных бактерий – сопрягающие
мембраны.
На самом деле, пластиды и митохондрии
имеют сопрягающую мембрану.
Для всех сопрягающих
мембран характерны особенности, которые
отличают эту мембрану от других мембран
эукариотических клеток:
1) Сопрягающие
мембраны способны синтезировать
АТФ за счет
внешних ресурсов.
2) Сопрягающие
мембраны несут цепь
переноса электронов.
3) Сопряженные
мембраны имеют специальные «грибовидные»
тельца, в которых находится фермент,
обеспечивающий синтез молекул АТФ с
названием АТФ-синтетаза.
4) Во всех сопрягающих
мембранах содержится повышенная
концентрация белков и низкая концентрация
холестерина.
Преобладающим
фосфолипидом в этих мембранах является
кардиолипин, наличие которого обуславливает
крайне низкую
избирательную способность.
Основой для
связывания двух биохимических процессов,
протекающих на сопрягающей мембране
является мембранный потенциал, который
создается на сопрягающей мембране.
Могут ли митохондрии передвигаться?