Для отделения митохондрий от гиалоплазмы служит наружная митохондриальная мембрана. Она, как правило, имеет ровные контуры и представляет собой замкнутый мембранный мешок. Между внешней и внутренней митохондриальными мембранами находится межмембранное пространство шириной около 10-20 нм.
Материал из «Знание.Вики»
Электронная микрофотография митохондрий
Митохо́ндрия — двумембранная органелла, которая преобразует энергию, получаемую из разложения различных органических соединений, в синтетическую энергию, необходимую для нормального функционирования клетки и процессов роста. Они используют аденозинтрифосфат (АТФ) и химические вещества, чтобы получить электроны, которые затем используются для восстановления энергии. Митохондрии характерны для большинства эукариотических клеток, как автотрофов (фотосинтезирующие растения), так и гетеротрофов (грибы, животные).
Биохимические процессы в митохондриях начинаются с транспорта субстратов через митохондриальную мембрану, который осуществляется с помощью транспортных белков — транслоказ, служащих переносчиками дикарбоновых кислот, АТФ и AДФ. Основные субстраты митохондрий — пируват и жирные кислоты, которые транспортируются с помощью карнитин-пальмитоил-трансферазы и карнитина.
Утилизация жирных кислот происходит в процессе β-окисления, а центральный путь утилизации углеродсодержащих молекул осуществляется через цикл Кребса. В результате этого цикла также образуются молекулы никотинамидадениндинуклеотидов (НАД) и флавинадениндинуклеотидов (ФАД), передающие свои электроны в дыхательную цепь митохондрий. Дыхательная цепь митохондрий состоит из пяти мультиферментных комплексов, которые находятся под генетическим контролем как митохондриального, так и ядерного генома.
Данная статья имеет статус «готовой». Это не говорит о качестве статьи, однако в ней уже в достаточной степени раскрыта основная тема. Если вы хотите улучшить статью — правьте смело!
Митохондрии — это органеллы размером с бактерию (около 1×2 мкм). Они найдены в большом количестве почти во всех эукариотических клетках. Обычно в клетке содержится около 2 000 митохондрий, общий объем которых составляет до 25 % от общего объёма клетки. Митохондрия ограничена двумя мембранами — гладкой внешней и складчатой внутренней, имеющей очень большую поверхность. Складки внутренней мембраны глубоко входят в матрикс митохондрий, образуя поперечные перегородки — кристы. Пространство между внешней и внутренней мембранами обычно называют межмембранным пространством.
Различные типы клеток отличаются друг от друга как по количеству и форме митохондрий, так и по количеству крист. Особенно много крист имеют митохондрии в тканях с активными окислительными процессами, например в сердечной мышце. Вариации митохондрий по форме, что зависит от их функционального состояния, могут наблюдаться и в тканях одного типа. Митохондрии — изменчивые и пластичные органеллы.
Мембраны митохондрий содержат интегральные мембранные белки. Во внешнюю мембрану входят порины, которые образуют поры и делают мембраны проницаемыми для веществ с молекулярной массой до 10 кДа (см. Транспортные белки). Внутренняя же мембрана митохондрий непроницаема для большинства молекул; исключение составляют O2, CO2, H2O. Внутренняя мембрана митохондрий характеризуется необычно высоким содержанием белков (75 %). В их число входят транспортные белки-переносчики (см. Транспортные системы), ферменты, компоненты дыхательной цепи и АТФ-синтаза. Кроме того, в ней содержится необычный фосфолипид кардиолипин (см. Фосфолипиды и гликолипиды). Матрикс также обогащён белками, особенно ферментами цитратного цикла.
Статьи раздела «Митохондрии
Схема строения митохондрии
Внутренняя мембрана представляет собой фосфолипидный бислой, содержащий комплексы окислительного фосфорилирования, входящие в состав дыхательной цепи и локализованных на кристах. Дыхательная цепь включает в себя IV белковых комплексов и АТФ-синтазу. Эти белковые комплексы имеют следующий состав: белковый комплекс I (NADH: Кофермент Q оксидоредуктаза) , белковый комплекс II (сукцинат: кофермент Q оксидоредуктаза), белковый комплекс III (кофермент Q: цитохром С оксидоредуктаза) и белковый комплекс IV (цитохром с-оксидаза).
В матриксе происходят различные биохимические процессы.
Этот процесс генерирует большое количество энергии, запасаемых в виде молекул АТФ.
Электронтранспортная цепь митохондрий является местом проведения окислительного фосфорилирования у эукариот. NADH и сукцинат, образовавшиеся в ходе цикла трикарбоновых кислот, окисляются, и их энергия передаётся АТФ-синтазе, которая за её счёт синтезирует АТФ.
Митохо́ндрия (от греч. μίτος – нить и χόνδριον – зёрнышко, крупинка), внутриклеточная органелла эукариотических клеток, основная функция которой – генерация энергии. Впервые митохондрии описаны немецким учёным Р. Альтманом (1894), который считал их элементарными организмами («биобластами»), живущими внутри клеток и осуществляющими жизненно важные функции. В 1898 г. немецкий гистолог К. Бенда дал им название «митохондрии». К середине 20 в. была предложена гипотеза о происхождении митохондрий, в соответствии с которой их появление в ходе эволюции эукариот является результатом симбиоза последних с аэробными бактериями.
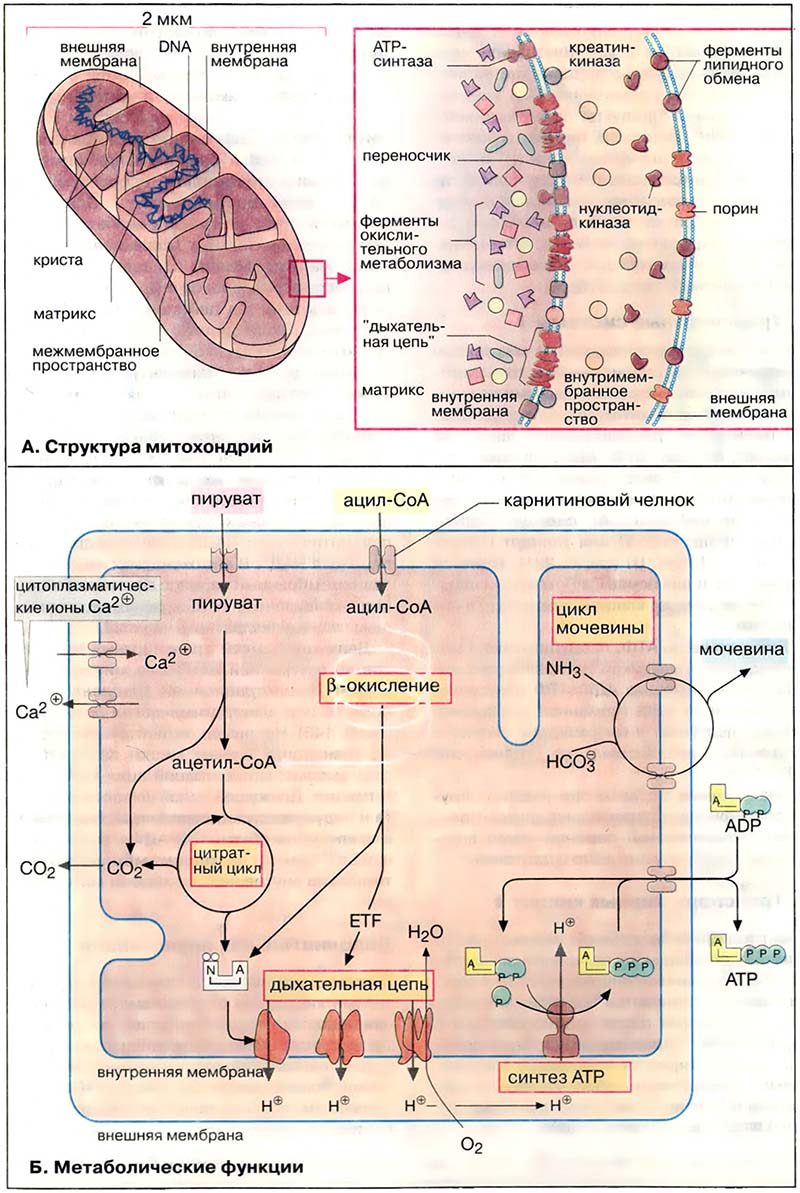
Структура митохондрий
Митохондрии – изменчивые и пластичные органеллы. Их количество в клетках, размеры и форма могут различаться в зависимости от функционального статуса клетки, стадии развития организмов. Форма митохондрий варьирует от почти круглой до сильно вытянутой, имеющей вид нити (в нейроне, например, их длина достигает 60 мкм) и сильно разветвлённой (в поперечно-полосатых мышцах).
Структура митохондрий универсальна. В них различают матрикс – внутреннее пространство, отграниченное от содержимого клетки (цитоплазмы) складчатой внутренней и гладкой внешней мембранами, между которыми находится межмембранное пространство.
В матриксе сосредоточен собственный генетический аппарат митохондрий, обычно представленный несколькими копиями кольцевой молекулы митохондриальной ДНК (мтДНК), компоненты, необходимые для транскрипции и трансляции белков, кодируемых митохондриальным геномом, ферменты цикла трикарбоновых кислот, бета-окисления жирных кислот, другие общие, а также специфичные для определённых типов клеток белки и ферменты. Однако бо́льшая часть генов, кодирующих митохондриальные белки, локализована в хромосомах ядра (в том числе гены большинства рибосомных белков и все факторы трансляции). мтДНК у растений в 30–100 раз больше, чем у животных.
Выявлены отличия генетического кода в митохондриях от генетического кода прокариот и эукариот (4 из 64 кодонов имеют другие значения); для синтеза белка используются лишь 22 (вместо 31) транспортные РНК. В митохондриях правила кодон-антикодонового спаривания менее строгие, что снижает точность белкового синтеза. У млекопитающих (в том числе у человека) митохондриальные гены наследуются по материнской линии.
Внутренняя мембрана митохондрий образует глубоко входящие в матрикс многочисленные выпячивания – кристы, увеличивающие площадь её контакта с матриксом. Форма крист варьирует у разных объектов, их число коррелирует с потребностями клетки в энергии (их очень много, например, в митохондриях сердечной мышцы). В ней локализованы многочисленные ферменты, компоненты дыхательной цепи митохондрий.
Внутренняя мембрана митохондрий непроницаема для большинства молекул; транспорт большей части веществ внутрь митохондрий и из неё осуществляют локализованные в ней специализированные транспортные системы (например, адениннуклеотидтранслоказа участвует в переносе аденозиндифосфата внутрь митохондрий, а аденозинтрифосфата (АТФ) из митохондрий в цитоплазму).
Компоненты дыхательной цепи обеспечивают многоступенчатую передачу электронов по цепи переносчиков – последовательное окисление и восстановление её компонентов, приводя в конечном итоге к восстановлению O2. Одновременно происходит перемещение протонов H+ из матрикса в межмембранное пространство и формирование протонного градиента, энергия которого используется для синтеза АТФ.
Во внешней мембране митохондрий локализованы белки, выполняющие самые разнообразные функции: интегральные белки порины и транслоказы, обеспечивающие её проницаемость для множества веществ, в том числе и белков; ферменты, участвующие в катаболизме ряда соединений (например, моноаминоксидаза – в распаде многих аминов, кинуренин-3-монооксигеназа – в деградации триптофана) и т. п.
Внутренняя и внешняя мембраны формируют контактные участки, необходимые для транспорта различных веществ, а также для слияния и деления митохондрий. В межмембранном пространстве содержатся белки-шапероны, участвующие в правильном встраивании белков в мембраны этих органелл, специальные факторы, которые поступают в цитоплазму при апоптозе, белки, участвующие в энергетическом обмене и динамических изменениях структуры митохондрий.
Функции митохондрий
Было доказано, что основная функция митохондрий связана с процессами окисления органических веществ, сопряжённого с синтезом макроэргического соединения – АТФ.
Митохондрии называют энергетическими станциями клетки, поскольку помимо генерации энергии, которая может расходоваться в виде тепла, в процессах биосинтеза, транспорте ионов и др., они являются одним из основных внутриклеточных депо ионов кальция, играют важную роль в регуляции метаболизма. Митохондрии ряда клеток участвуют в синтезе стероидных гормонов из холестерина, синтезе гема и других веществ.
При изменении структурной организации митохондрий может происходить формирование дополнительных каналов (пор) и выделение в цитозоль белковых факторов, инициирующих апоптоз. Нарушения структуры и функций митохондрий обнаружены при различных патологических состояниях организма человека, включая рак, болезни Альцгеймера и Паркинсона. Мутации в ядерном и особенно в митохондриальном геномах приводят к развитию различных нейродегенеративных расстройств (мышечные дистрофии, некоторые виды энцефалопатий и др.), которые прежде всего обусловлены нарушением энергетических функций митохондрий.
Локализация митохондрий в клетке
Общее число митохондрий в клетке колеблется от одной гигантской (у одноклеточных зелёных водорослей и простейших) до тысячи (в клетках млекопитающих). В клетках зелёных растений митохондрий меньше, чем в клетках животных; в молодых клетках они более многочисленны, чем в стареющих.
Митохондрии могут равномерно распределяться в цитоплазме либо локализоваться группами в местах, где возникает потребность в источнике энергии (например, у основания жгутиков сперматозоидов, вблизи миофибрилл скелетных мышц).
В живых клетках митохондрии могут перемещаться (с помощью белков кинезинов и микротрубочек), сливаться друг с другом. Увеличение числа митохондрий происходит путём их деления.
Опубликовано 18 сентября 2023 г. в 09:00 (GMT+3). Последнее обновление 18 сентября 2023 г. в 09:00 (GMT+3).
ОБЗОР ОКИСЛИТЕЛЬНЫХ ВОЗМОЖНОСТЕЙ МИТОХОНДРИАЛЬНОГО
ЭНЕРГЕТИЧЕСКОГО АППАРАТА Цехомский А.В.1, Малай Д.А.2
1Цехомский Александр Вячеславович-студент; 2Малай Дмитрий Александрович-студент, лечебный факультет, Кубанский государственный медицинский университет, г. Краснодар
Аннотация: митохондрии имеют широкие “полномочия” по окислению различных субстратов. Окисление происходит на специфических органеллах митохондрий – кристах, которые образуют окислительный аппарат. Кристы содержат особые структуры, на которых находится огромное количество ферментов. Ферментативная совокупность оказывает особое влияние на субстратные комплексы, расщепляя и гидролизуя их. Но гидролиз – не единственный механизм преобразования субстрата. В статье будут подробно рассмотрены механизмы видоизменения таких субстратных единиц, как белки и низкомолекулярные соединения(глюкоза и витамины). Помимо этого будут рассмотрены особенности использования энергии митохондриями для совершения окислительных процессов и запасания энергии в форме универсального переносчика – аденозинтрифосфата(АТФ) и использования своих терморегуляторных функций – выделения тепла во внешнюю среду. Результатом работы станет подробный обзор функций энергетического аппарата митохондрий в клетках эукариот.
Ключевые слова: митохондрии, энергетический аппарат, АТФ, кристы, механизм, гидролиз.
1. Виды субстратов, используемые митохондриями.
Итак, в митохондриях выделяют несколько главных энергетических субстратов:
2. Механизмы преобразования субстратных единиц.
А). Механизмы преобразования длинноцепочечных жирных кислот (ДЦ-ЖК).
Последующий алгоритм переноса и преобразования ДЦ-ЖК из саркоплазмы в митохондрии будет делится на ряд последовательных этапов:
Б). Механизмы преобразований глюкозы.
В). Механизмы преобразований лактата (аниона молочной кислоты).
3. Откуда митохондрии берут энергию для гидролиза?
Таким образом, происходит образование молекул АТФ в митохондриях кардиомиоцитов. Следует отметить, что цикл трикарбоновых кислот для всех клеток нашего организма одинаков и не носит специфического характера в отдельных тканях.
Подводя итог к проведенному обзору, можно сделать однозначный вывод: митохондрии являются важным энергетическим комплексом эукариотических клеток. Количество митохондрий и интенсивность
выработки молекул АТФ прямо пропорционально зависит от специфической функции той или иной
1. Энтони Л. Мешер «Гистология по Жункейре», учебное пособие, атлас. ИЗДАТЕЛЬСКАЯ ГРУППА «ГЭОТАР-Медиа» 2022 г.,
2. Mitochondrial electron transport chain: Oxidative phosphorylation, oxidant production, and methods of measurement; Deirdre Nolfi-Donegan, Andrea Braganza, Sruti Shiva, Redox Biology, Volume 37, 2020, 101674, ISSN 2213-2317, https://doi.org/10.1016/j.redox.2020.101674.
3. Galactose enhances oxidative metabolism and reveals mitochondrial dysfunction in human primary muscle cells. Aguer, C., Gambarotta, D., Mailloux, R. J., Moffat, C., Dent, R., Mcpherson, R., et al. (2011). PLoS One 6: e28536. doi: 10.1371/ journal.pone.0028536
4. The histone demethylase KDM4B interacts with MyoD to regulate myogenic differentiation in C2C12 myoblast cells. Choi, J. H., Song, Y. J., and Lee, H. (2015). Biochem. Biophys. Res. Commun. 456, 872878. doi: 10.1016/j.bbrc.2014. 12.061
5. Acetylated histone H3K56 interacts with Oct4 to promote mouse embryonic stem cell pluripotency. Tan, Y., Xue, Y., Song, C., and Grunstein, M. (2013). Proc. Natl. Acad. Sci. U.S.A. 110, 11493-11498. doi: 10.1073/pnas.130991 4110
6. Creatine supplementation prevents the inhibition of myogenic differentiation in oxidatively injured C2C12 murine myoblasts. Sestili, P., Barbieri, E., Martinelli, C., Battistelli, M., Guescini, M., Vallorani, L., et al. (2009). Mol. Nutr. Food Res. 53, 1187-1204. doi: 10.1002/mnfr.200800504
7. Mitochondrial Function in Muscle Stem Cell Fates. Bhattacharya D and Scime A (2020) Front. Cell Dev. Biol. 8:480. doi: 10.3389/fcell.2020.00480
8. Опыт применения триметазидина МВ у больных с хронической сердечной недостаточностью. Морозова Т.Е., Иванова Е.П. Кардиоваскулярная терапия и профилактика. 2010. Т. 9. № 3. С. 45-51
9. Новые возможности триметазидина МВ в лечении ишемической болезни сердца в условиях реальной клинической практики. Результаты Российского многоцентрового, рандомизированного исследования ПЕРСПЕКТИВА (часть II). Бубнова М.Г., Аронов Д.М., Оганов Р.Г., Рудоманов О.Г. Кардиоваскулярная терапия и профилактика. 2011. Т. 10. № 6. С. 70-80
10. Клиническая характеристика и общие подходы к лечению пациентов со стабильной стенокардией в реальной практике. Российское исследование ПЕРСПЕКТИВА (часть I). Бубнова М.Г., Аронов Д.М., Оганов Р.Г., Рудоманов О.Г., Путылина А.С. Кардиоваскулярная терапия и профилактика. 2010. Т. 9. № 6. С. 47-56
11. Цитопротективное влияние триметазидина на острый коронарный синдром (отдаленные результаты): диссертация на соискание ученой степени кандидата медицинских наук: код специальности 14.01.05 Кардиология: защищена 15.09.2015 / Васильев Сергей Владимирович; науч. рук. Майчук Елена Юрьевна; ГБОУ ВПО “Московский государственный медико-стоматологический университет им. А. И. Евдокимова”. — Москва, 2015. — 155 с.: ил., табл.; 31. — Фондодержатель ЦНМБ.
13. Korobova, F., Ramabhadran, V., and Higgs, H. N. (2013). An Actin- dependent Step in Mitochondrial Fission Mediated by the ER-Associated Formin INF2. Science 339 (6118), 464-467. doi: 10.1126/science. 1228360
14. HoodD.A., Memme J.M., Oliveira A.N., and Triolo M. (2019).
15. Maintenance of Skeletal Muscle Mitochondria in Health, Exercise, and
16. Aging. Annu. Rev. Physiol. 81, 19-41. doi:10.1146/annurev-physiol
17. Spaniol M., Kaufmann P., Beier K., et al. Mechanisms of liver sreatosis in rat with systemic carnitine deficiency due to treatment with trimethylhydrazini Umpropionate. J Lipid Research 2003; 44: 144-53.
18. Cho B., Cho H.M., Jo Y., Kim H.D., Song M., Moon C., et al. (2017). Constriction of the Mitochondrial Inner Compartment Is a Priming Event for Mitochondrial Division. Nat. Commun. 8, 15754. doi: 10.1038/ncomms15754
19. De La Fuente S., Fernandez-Sanz C., Vail C., Agra E. J., Holmstrom K., Sun J., et al. (2016). Strategic Positioning and Biased Activity of the Mitochondrial Calcium Uniporter in Cardiac Muscle. J. Biol. Chem. 291 (44), 23343-23362. doi: 10.1074/jbc.m116.755496
20. Hidalgo M., Marchant D., Quidu P., Youcef-Ali K., Richalet J.P., Beaudry M., et al. (2014). Oxygen Modulates the Glutathione Peroxidase Activity during the L6 Myoblast Early Differentiation Process. Cell Physiol Biochem 33 (1), 67-77. doi: 10.1159/000356650
21. Mailloux R.J. (2018). Mitochondrial Antioxidants and the Maintenance of Cellular Hydrogen Peroxide Levels. Oxid Med. Cel Longev 2018, 7857251. doi: 10.1155/2018/7857251
22. Henriquez-Olguin C., Meneses-Valdes R., and Jensen T. E. (2020). Compartmentalized Muscle Redox Signals Controlling Exercise Metabolism – Current State, Future Challenges. Redox Biol. 35, 101473. doi: 10.1016/j.redox. 2020.101473
23. Fonseca T.B., Sánchez-Guerrero A., Milosevic I., and Raimundo N. (2019). Mitochondrial Fission Requires DRP1 but Not Dynamins. Nature 570 (7761), E34-E42. doi:10.1038/s41586-019-1296-y
24. Eisner V., Lenaers G., and Hajnóczky G. (2014). Mitochondrial Fusion Is Frequent in Skeletal Muscle and Supports Excitation-Contraction Coupling. J. Cel Biol 205 (2), 179-195. doi: 10.1083/jcb.201312066
25. Calvani R., Joseph A.-M., Adhihetty P.J., Miccheli A., Bossola M.1. Leeuwenburgh C., et al. (2013). Mitochondrial Pathways in Sarcopenia of
26. Aging and Disuse Muscle Atrophy. Biol. Chem. 394 (3), 393-414.doi:10.1515/ hsz-2012-0247
27. Nagdas S., and Kashatus D.F. (2017). The Interplay between Oncogenic Signaling Networks and Mitochondrial Dynamics.Antioxidants (Basel)6 doi:10.3390/antiox6020033
28. Cogliati S., Enriquez J.A., and Scorrano L. (2016). Mitochondrial Cristae: Where Beauty Meets Functionality. Trends Biochem. Sci. 41 (3), 261-273. doi: 10.1016/ j.tibs.2016.01.001
29. Bernardi, P. (2019). Mitochondrial H+ Permeability through the ADP/ATP Carrier. Nat. Metab. 1 (8), 752-753. doi: 10.1038/s42255-019-0079-y
30. Bhatti J.S., Bhatti G.K., and Reddy P.H. (2017). Mitochondrial Dysfunction and Oxidative Stress in Metabolic Disorders – A Step towards Mitochondria Based Therapeutic Strategies. Biochim. Biophys. Acta (Bba) – Mol. Basis Dis. 1863 (5), 1066-1077. doi:10.1016/j.bbadis.2016.11.010
31. Nicholls D.G. (2009). Spare Respiratory Capacity, Oxidative Stress and Excitotoxicity. Biochem. Soc. Trans. 37 (Pt 6), 1385-1388. doi: 10.1042/BST0371385
32. Jezek J., Cooper K.F., and Strich R. (2018). Reactive Oxygen Species and Mitochondrial Dynamics: The Yin and Yang of Mitochondrial Dysfunction and Cancer Progression. Antioxidants (Basel) 7 (1).
Митохондрии – это органеллы, которые присутствуют практически во всех эукариотических клетках. Их основная, но не единственная функция — производство энергии.
Что такое митохондрии
Митохондрии — клеточные органеллы, расположенные вне ядра, а именно в цитоплазме. Они отвечают за выработку большей части энергии, необходимой для запуска биохимических реакций в клетке. Энергия, вырабатываемая митохондриями, хранится в небольшой молекуле, называемой аденозинтрифосфатом (АТФ).
Процессы внутри митохондрий осуществляются точным механизмом, в котором задействованы различные белки, молекулы, каналы и мембраны. Он настолько развит, что даже высказывалось предположение, что этот механизм произошел от прокариотической клетки, поглотившей аэробные бактерии миллионы лет назад.
Одной из основных характеристик митохондрий является то, что они содержат собственные небольшие хромосомы, то есть, содержат гены, отдельные от тех, что находятся в ядре клетки. Эти гены наследуются только от матери, в отличие от ядерных генов, которые наследуются от обоих родителей.
Количество митохондрий варьируется в зависимости от типа клетки, поскольку некоторым органам и тканям требуется гораздо больше энергии, например, мышцам, мозгу или печени.
Семинары по антивозрастной медицине
Получайте знания, основанные на доказательной медицине из первых уст ведущих мировых специалистов. В рамках Модульной Школы Anti-Age Expert каждый месяц проходят очные двухдневные семинары, где раскрываются тонкости anti-age медицины для врачей более 25 специальностей
Строение
Морфология митохондрий весьма изменчива и может варьировать от длинных разветвленных структур до небольших эллипсоидов. Можно сказать, что существуют отдельные митохондрии и динамические митохондриальные сети. Сетевые или изолированные митохондрии состоят из внешней и внутренней мембран, межмембранного и внутреннего пространства, ограниченного внутренней мембраной, называемого митохондриальным матриксом.
Внешняя мембрана митохондрий обладает высокой проницаемостью и содержит множество копий белка порина, который образует водные каналы через липидный бислой. Таким образом, эта мембрана становится своего рода ситом, проницаемым для всех молекул размером менее 5000 дальтон, включая небольшие белки.
Внутренняя мембрана образует матрикс. Это аналог цитоплазмы клетки. Энергия поступает из этого региона в виде АТФ. Здесь происходят обменные процессы, такие как:
Именно здесь расположены другие микроорганеллы митохондрий, такие как рибосомы, ДНК, ионы и метаболиты. Внутренняя мембрана состоит из липидного бислоя, в котором находятся ферментные комплексы, состоящие из различных белков, необходимых для цепи переноса электронов.
Наружная и внутренняя мембраны представляют собой части митохондрий, которые складываются в кристы в виде складок. Они расположены преимущественно по краям митохондрий, но отграничены снаружи внешней мембраной. Они расположены перпендикулярно границе митохондрий.
Кристы образуют отдельный отсек от остальной части внутренней мембраны, поскольку содержание белка в них сильно отличается. Считается, что количество и форма митохондриальных крист являются отражением клеточной активности. В кристах обнаружены функциональные дыхательные комплексы и АТФ-синтаза, а также белки для сборки железо-серных групп. Гребни позволяют значительно увеличить площадь поверхности для размещения белков дыхательной цепи и АТФ. В клетке печени внутренняя митохондриальная мембрана может составлять 1/3 общей клеточной мембраны.
В мембранах крист происходят важнейшие функции митохондрий:
Между внутренней и внешней мембраной имеется пространство, называемое митохондриальным межмембранным пространством, которое имеет жизненно важное значение для клеточной активности. В нем – высокое содержание ферментов, необходимых для дыхания. Его основная функция – прием протонов от перекачки ферментных комплексов. Здесь присутствуют ферменты и белки, которые помогают в клеточных процессах. Здесь также происходит транслокация — процесс, при котором белки митохондриального матрикса транспортируются извне митохондрий. Наконец, они транспортируют жирные кислоты.
Митохондрии также имеют рибосомы, называемые миторбосомами или митохондриальными рибосомами. Их функция – синтез белков посредством трансляции генов. Они получают информацию в виде РНК, чтобы перевести ее в ДНК.
В митохондриальном матриксе также есть ДНК и ферменты, осуществляющие метаболические процессы. Митохондриальная ДНК находится в местах, называемых нуклеоидами, и каждый нуклеоид может содержать более одной молекулы ДНК. Нуклеоиды связаны с внутренней мембраной митохондрий посредством белкового комплекса MitOS. Также в нуклеоиде имеются белки для репликации и восстановления митохондриальной ДНК. Обычно он содержит около 16 500 пар оснований и около 37 генов, которые у человека кодируют 13 белков. Внутри клетки могут находиться сотни копий митохондриальной ДНК. Репликация митохондриальной ДНК не связана с клеточным циклом, и в любой момент жизни клетки может произойти репликация этой ДНК.
Митохондрии, или части митохондриальной сети, перемещаются из одной части клетки в другую и обычно располагаются там, где существует наибольшая потребность в энергии или кальции.
Основная функция митохондрий — производство АТФ, который является топливом для большинства клеточных процессов. Но они также осуществляют часть метаболизма жирных кислот посредством процесса, называемого β-окислением, и действуют как депо кальция, образование гемовых групп, синтез аминокислот и биогенез железосульфидных групп.
Большая часть АТФ в нефотосинтезирующих эукариотических клетках производится в митохондриях. Они метаболизируют ацетил-коэнзим А посредством ферментативного цикла лимонной кислоты, давая в качестве продуктов CO2 и НАДН.
Именно НАДН отдает электроны цепочке переносчиков электронов, находящихся в мембранах крист митохондрий. Эти электроны переходят от одного носителя к другому, достигая на последнем этапе O2, в результате чего образуется H2O. Этот транспорт электронов связан с транспортировкой протонов из матрицы во внутреннее пространство гребня. Именно этот протонный градиент позволяет синтезировать АТФ благодаря АТФ-синтазе. Этот процесс, в котором фосфат связывается с АДФ и кислород используется в качестве конечного акцептора электронов, который называется окислительным фосфорилированием. Белки, осуществляющие транспорт электронов и АТФ-синтазу, находятся в кристах митохондрий и могут достигать до 80% массы митохондриальной мембраны.
Цепь переноса электронов известна как дыхательная цепь. Она содержит около 40 белков, из которых 15 непосредственно участвуют в транспорте электронов. Все эти белки объединены в три комплекса, каждый из которых содержит несколько белков. Они называются: комплекс НАДН-дегидрогеназы, комплекс цитохрома b-c1 и комплекс цитохромоксидазы. У каждого из них есть химические группы, которые позволяют проходить через них протонам, перемещаемым за счет транспорта электронов.
Производство энергии в митохондриях представляет собой двухэтапный процесс: создание протонного градиента между обеими сторонами мембраны митохондриального гребня, создаваемого цепью переноса электронов, и синтез АТФ АТФ-синтазой, которая использует это преимущество. Оба процесса связаны с митохондриальными кристами.
В результате в матриксе создается градиент протонов в 10 раз меньший, чем в межмембранном пространстве. Кроме того, в матрице создается более отрицательно заряженное пространство вследствие чистого ухода положительных зарядов по отношению к межмембранному пространству, которое становится более положительным. Создается электрохимический градиент, который заставляет протоны стремиться вернуться в матрицу.
Синтез АТФ — не единственный процесс, в котором используется протонный градиент. Другие заряженные молекулы, такие как пируват, АДФ и неорганический фосфор, перекачиваются в матрикс из цитозоля, тогда как другие, такие как АТФ, синтезируемая в матриксе, должны транспортироваться в цитозоль. Неорганический фосфор и пируват транспортируются путем соединения с входящим потоком протонов в рамках сопутствующего котранспорта. С другой стороны, АДФ связан котранспортом антипортового типа с АТФ.
Значительный синтез клеточных липидов происходит в митохондриях. Вырабатывается лизофосфатидная кислота, из которой синтезируются триацилглицерины. В митохондриях также синтезируются фосфатидная кислота и фосфатидилглицерин, последний необходим для продукции кардиолипина и фосфатидилэтаноламина.
Существуют органеллы, возникшие из митохондрий в ходе эволюции и приобретшие другие функции. Например, гидрогеносомы связаны с метаболизмом водорода, а митосомы — с метаболизмом серы. В этих органеллах отсутствует ДНК. С другой стороны, в последнее время митохондрии вместе с эндоплазматическим ретикулумом участвуют в генерации пероксисом посредством эмиссии везикул.
В ситуациях стресса митохондрии способны вызвать реакцию, направленную на защиту от указанного стресса. Однако если стрессовая ситуация затягивается и нанесенный ею ущерб не может быть устранен, запускается процесс регулируемой гибели клеток, называемый апоптозом. Внутриклеточный путь активации апоптоза требует участия митохондрий. Апоптоз также задействован в морфогенетических и физиологических процессах.
Синтез и деление
Митохондрии обладают способностью относительно легко делиться и сливаться, и эти два действия постоянно происходят в клетках. Это включает в себя смешивание и деление митохондриальной ДНК каждой из этих единиц органелл.
В эукариотических клетках нет отдельных митохондрий, а есть сеть, связанная с переменным количеством митохондриальной ДНК. Одна из возможных функций этого явления — делиться продуктами, синтезируемыми разными частями сети, исправлять локальные дефекты или просто делиться своей ДНК.
Если две клетки с разными митохондриями сливаются, сеть митохондрий, возникшая в результате объединения, станет однородной уже через 8 часов.
Деление митохондрий опосредовано белками, очень похожими на динамины , которые участвуют в образовании везикул. Точка, в которой эти органеллы начинают делиться, во многом зависит от их взаимодействия с эндоплазматической сетью. Мембраны ретикулума окружают митохондрии, сжимая их и в конечном итоге разделяя на две части.
Митохондрии и старение
Митохондрии управляют правильным функционированием клеток, обеспечивая их топливом (АТФ). Они также регулируют апоптоз – «самоубийство» клетки, когда она слишком повреждается или стареет. Таким образом, наши “энергетические станции” предотвращают накопление стареющих клеток в наших тканях, что является одной из основных причин старения.
Существуют исследования, которые показали, что возрастные заболевания связаны со снижением способности клеток вырабатывать энергию.
Митохондриальное истощение приводит к ухудшению иммунной защиты, нарушениям продукции гормонов, ухудшению пищеварения, недостаточной детоксикации печени, мышечной слабости и так далее.
Падение выработки гормона прегненолона также может быть признаком низкой активности митохондрий, вырабатывающих его из холестерина. Прегненолон является предшественником ДГЭА.
Кроме того, многие ученые считают, что продолжительность жизни человека связана с количеством у него митохондрий. Можно сказать, что наша жизнеспособность во многом зависит от состояния наших митохондрий.
По мере старения, особенно в случае чрезмерно интенсивных явлений окисления, митохондриальная ДНК легче повреждается и мутирует. Поврежденные митохондрии производят меньше энергии, но больше свободных радикалов, чем обычно, и способствуют воспалению, болезням и старению.
Таким образом, плохое функционирование митохондрий может привести к раку, ускоренному старению, дегенеративным заболеваниям, хроническому воспалению и накоплению внутриклеточных токсинов. Кроме того, в борьбе со старением особенно важно обеспечить функциональность и здоровье митохондрий.
ВАЖНО: эпигенетика и, следовательно, наш образ жизни влияют на митохондриальную ДНК и в то же время на деление наших клеток и поддержание их здоровья.
Факторы, повреждающие митохондрии
Митохондриальная дисфункция является наиболее частой причиной заболеваний и дегенеративных расстройств в нашем обществе, связанных с образом жизни. Различают первичные или врожденные митохондриальные нарушения, вызванные мутациями, и вторичные или приобретенные, обусловленные дефицитом выработки энергии или АТФ.
Факторы, предрасполагающие к повреждению митохондрий:
Как улучшить работу митохондрий
Митохондрии обладают способностью саморегулироваться в клетке, чтобы улучшить выработку энергии в конечном итоге увеличить процент здоровых и продуктивных митохондрий.
Несколько митохондрий могут объединяться с образованием более эффективных митохондрий (этому благоприятствует снижение потребления питательных веществ, голодание и т. д.), а также митохондрия может делиться на несколько более мелких, менее эффективных. Это происходит в случае, когда потребление питательных веществ слишком велико.
К этим регуляторным процессам добавляется функция, аналогичная аутофагии, позволяющая восстанавливать или устранять слишком поврежденные митохондрии, что активируется ограничением (рестрикцией) калорий.
В конечном счете производство энергии более эффективно при ограничении питательных веществ , чем при их избытке (по крайней мере, в определенной степени).
Нам также следует избегать подачи слишком большого количества питательных веществ в митохондрии, иначе мы рискуем вызвать ненужное окисление в наших клетках.
Фактически, забота о митохондриях сейчас становится одним из приоритетов в борьбе с последствиями старения.
Существует несколько способов активировать митохондрии:
Сжигание питательных веществ в митохондриях происходит с участием кислорода. Любая физическая активность, движение, техника дыхания могут помочь оптимизировать подачу кислорода. Также важно поддерживать хорошее кровообращение.
В производстве митохондриальной энергии участвуют различные необходимые питательные вещества. Поэтому необходимо избегать их дефицита. Каких именно витаминов и микроэлементов не хватает организму, может с высокой точностью определить доктор антивозрастной медицины, который при необходимости назначит добавки.
Онлайн обучение
Anti-Age медицине
Изучайте тонкости антивозрастной медицины из любой точки мира. Для удобства врачей мы создали обучающую онлайн-платформу Anti-Age Expert: Здесь последовательно выкладываются лекции наших образовательных программ, к которым открыт доступ 24/7. Врачи могут изучать материалы необходимое количество раз, задавать вопросы и обсуждать интересные клинические случаи с коллегами в специальных чатах





