- Конкурс «Био/Мол/Текст»-2020/2021
- Нарушение работы митохондрий (митохондриальная дисфункция)
- Митохондрии и мозг
- Митохондрии и иммунитет
- Так как же вылечить митохондрии?
- Митохондриальная обогащающая терапия
- Трансфер выделенных изолированных митохондрий непосредственно в ткань или системно в кровоток
- Можно ли вылечить митохондрии?
- Митохондриальная медицина развивается!
- А ну-ка все на диагностику!
- Всех построим в ряд
- А ну-ка глянем, что там?
- Может быть, стоит оказать на них влияние?
- Мишень — кардиолипин
- Скажи «нет» окислению!
- А если подправить гены?
- Митохондрии и психика
- Как можно помочь своим митохондриям
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Нарушение работы митохондрий (митохондриальная дисфункция)
К сожалению, побочным продуктом этой энергии является формирование огромного потока свободных радикалов. Свободные радикалы – это молекулы, которые имеют свободный электрон, что заставляет их реагировать с другими молекулами в нестабильных формах и делать это крайне разрушительно.
Свободные радикалы атакуют структуру наших клеточных мембран, создавая продукты обмена веществ, нарушающие производство ДНК и РНК, мешающие синтезу белка и разрушающие важные клеточные ферменты. Жизненно важные ткани и молекулы распадаются под воздействием свободных радикалов. Более того, разрушение клеточных механизмов свободными радикалами создает мутантные клетки, которые связаны с раком и старение.
Митохондрии – это самые легкие мишени для воздействия на них свободных радикалов по двум причинам
- Они находятся именно там, где эти свободные радикалы образуются.
- Им не хватает большей части антиоксидантной защиты, обнаруженной в других частях клетки.
Доказательств убедительно свидетельствует о том, что с течением времени происходит накоплений повреждений ДНК митохондрий, в частности, это ведет к нарушению обмена веществ (например, диабету) и к дегенеративным заболеваниям (таких как болезнь Альцгеймера).

ОРГАНЫ ТЕЛА, ПОДВЕРЖЕННЫЕ ЗАБОЛЕВАНИЯМ ПРИ УХУДШЕНИИ РАБОТЫ МИТОХОНДРИЙ
Нарушения в работе митохондрий (митохондриальная дисфункция) происходят главным образом в органах и тканях, которые имеют высокий спрос на энергию. Вот почему сердечно-сосудистые ткани и нейроны мозга являются одними из самых восприимчивых к воздействию.
Митохондрии и мозг
Основной потребитель энергии митохондрий — мозг: ему нужно в 10 раз больше кислорода и глюкозы, чем другим тканям. Потому дисфункция митохондрий еще и приводит к гибели нейронов, а гибель нейронов — к нейродегенерации и болезням Альцгеймера и Паркинсона, предполагают ученые.
Чтобы понять, как дисфункция митохондрий связана с болезнью Паркинсона, исследователи из Великобритании и Германии проанализировали состояние митохондрий и мозга здоровых пожилых людей и пожилых с болезнью Паркинсона. Сначала они взяли образцы мозга, тонко порезали и опустили в специальный краситель. Этот краситель связывается с одним из белков, который митохондрии используют для синтеза АТФ, — цитохромом С. Потом отмыли ткани мозга. Нейроны покрасились, но особенным образом: чем ярче окрас, тем больше цитохрома С в нейроне и тем здоровее митохондрии.
Яркие нейроны с большим количеством цитохрома С оказались у здоровых пожилых людей. У людей с болезнью Паркинсона нейроны окрасились не так ярко. Их митохондрии страдали от дефицита белка и хуже превращали кислород и глюкозу в энергию: у них попросту не хватало оборудования.
Возник новый вопрос: почему в митохондриях людей с болезнью Паркинсона так мало цитохрома С? Ученые предположили: ген митохондрий повредился так неудачно, что они не производят достаточно этого белка. Так и оказалось: информация потерялась, а почему — неизвестно. Поврежденные нейроны с неполным геномом были и у здоровых, и у больных пожилых людей. При Паркинсоне их просто было намного больше, а у здорового молодого человека — не было вовсе.
Как именно здоровье митохондрий влияет на нейроны? Исследовать мозг живого человека сложно, поэтому обратимся к исследованиям на мышах. Но сначала вспомним важную вещь: чтобы синтезировать АТФ, митохондрии добывают энергию из кислорода и еды. Но не вся эта энергия идет на синтез АТФ. Часть митохондрии тратят на обогрев тела, часть — на образование активных форм кислорода. А чтобы рассеивать энергию в виде тепла и согреть тело, у митохондрий есть специальные белки.
С этими белками и поиграли ученые, создав мышей с дефектами: одни не могли эффективно синтезировать белки для рассеивания тепла, другие — наоборот, синтезировали их больше обычного. Митохондрии мышей с недостатком белков-энергоотводов производили больше активных форм кислорода: энергии просто некуда было деться. У этих мышей еще и было меньше митохондрий в нейронах. То есть нейроны получали и больше вреда, и меньше энергии. Потом ученые использовали на мышах нейротоксин, который вызывает гибель нейронов и Паркинсон. Мыши с недостатком белков заболевали гораздо быстрее.
Митохондрии и иммунитет
Бактерия слилась с клеткой, стала производить для нее энергию — и стала митохондрией. Скорее всего, изначально эта бактерия обеспечивала хозяина еще и защитой. Активные формы кислорода она использовала, чтобы разрушить и переварить захваченные клеткой патогены — бактерии или вирусы. Возможно, именно это сотрудничество стало нашей иммунной системой.
Сейчас митохондрии помогают организму быстро и эффективно реагировать на травмы. Когда клетки повреждаются, высвобождается митохондриальная ДНК — и попадает в кровь. Митохондриальная ДНК похожа на бактериальную, поэтому организм считывает это как сигнал опасности и активирует иммунный ответ.
А еще митохондрии активируют иммунные клетки. Например — макрофаги. Когда макрофаги получают от организма сигнал, что в тело проник патоген, митохондрии макрофагов переквалифицируются из энергостанций в военные сооружения. Они перестают синтезировать АТФ и полностью переходят на синтез активных форм кислорода. Активные формы кислорода, во-первых, говорят организму, что самое время начать сражение с патогеном, а во-вторых, и сами могут его уничтожить.
Митохондрии активны и в Т-клетках. Это спецагенты иммунитета, которые проверяют другие клетки на наличие вирусов, а если находят заболевшие — уничтожают. Как и другие митохондрии, митохондрии Т-клеток сливаются друг с другом и, наоборот, разделяются, меняют форму и размер, чтобы адаптировать процесс производства энергии к состоянию организма. Когда все спокойно, они длинные: это помогает эффективнее работать и производить меньше активных форм кислорода. Но когда организм идентифицирует угрозу (это может быть физическая травма, например), митохондрии Т-клеток фрагментируются — и в крови становится много коротких сегментов митохондриальной ДНК. В таком состоянии митохондрии образуют больше активных форм кислорода и тем самым дают иммунитету понять, что пора действовать.
Так как же вылечить митохондрии?
Сегодня используется в основном консервативное лечение митохондриальных заболеваний, которые не помогают, если степень митохондриальной дисфункции высока или если есть врожденные митохондриальные заболевания. Нормальная работа митохондрий нарушается не только при митохондриальных заболеваниях, но также при болезнях Альцгеймера и Паркинсона, диабете, саркопении, инсулин-резистентности и при таких состояниях как инсульт, инфаркт миокарда, а еще в процессе старения организма. При этом известно, что доставка новых митохондрий или восстановление их пула может давать терапевтический эффект.
Перенос митохондрий in vivo выполняет целый ряд физиологических функций:
Что касается искусственного переноса митохондрий, тут можно выделить два основных подхода.
Митохондриальная обогащающая терапия
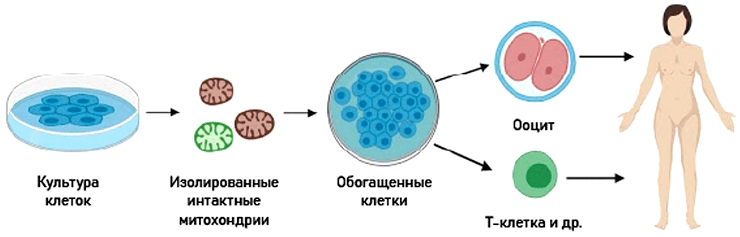
Рисунок 14. Принцип проведения митохондриальной обогащающей терапии
Для лечения митохондриальных заболеваний данный подход запатентовала и использует компания Minovia (Израиль). Пока что в исследование вовлечено пять пациентов с синдромом Пирсона.
Трансфер выделенных изолированных митохондрий непосредственно в ткань или системно в кровоток
В ходе развитие митохондриальной терапии потребуется решить еще немало вопросов. Например, очень важно оценить влияние системного и локального введения митохондрий на биомаркеры старения в животных моделях. Важно изучить, будет ли нормально реплицироваться ДНК пересаженных митохондрий, будут ли они способны к нормальному делению и другим процессам?
Ну и конечно, остается совершенствовать методологию. Очень нужно стандартизировать процедуры изоляции митохондрий, подобрать оптимальные концентрации для инъекции, тестировать среды, в которых находятся органеллы, и разработать методики оценки качества и целостности митохондрий. А еще важно выбрать оптимальный источник клеток и тканей для получения митохондрий. На данный момент, к сожалению, единого мнения насчет того, какой источник лучше всего, нет.
Можно ли вылечить митохондрии?
Термин «митохондриальная медицина» изначально возник в связи с исследованиями наследственных митохондриальных заболеваний. Сейчас это понятие расширилось и на возрастную дисфункцию митохондрий.
Митохондриальная медицина развивается!
А сейчас мы попробуем структурировать основные подходы митохондриальной медицины:
- Применение антиоксидантов.
- Митогормезис — запуск механизмов адаптации в ответ на стрессовое воздействие. При этом наблюдается адаптивное улучшение работы митохондрий.
- Стимуляция биогенеза митохондрий и процессов их динамики.
- Стимуляция митофагии.
- Оптимизация электрон-транспортной цепи митохондрий.
- Стабилизация липидов их внутренней мембраны.
- Трансплантация митохондрий.
- Генное редактирование митохондриальной ДНК.
Так как процессы, протекающие в митохондриях, взаимосвязаны, данные направления могут пересекаться. Например, стабилизация мембран митохондрий повышает качество процессов митофагии.
Кроме того, направления митохондриальной медицины можно подразделить на:
- диагностику функций митохондрий;
- консервативные подходы (изменение образа жизни);
- инновационные подходы (трансплантацию митохондрий, генную терапию митохондрий, перенос их генов в ядро и др.).
Видео 3. Понятие митохондриальной медицины. Методы диагностики дисфункции митохондрий. Генетические маркеры дисфункции. Методы консервативного поддержания работы митохондрий: спорт, питание, питательные вещества, антиоксиданты и другие подходы.
А ну-ка все на диагностику!
Качественная и достоверная диагностика митохондриальной дисфункции необходима и для разработки терапий, и для оценки их эффективности. Между тем, в этой области не существует стандартного набора методов. Зато существует ряд трудностей:
- Гетероплазмия. Так как клетки содержат разное количество митохондрий в зависимости от уровня метаболической активности ткани, в которой они находятся, генетический материал в этих митохондриях может быть различным. Некоторые из них могут нести мутацию, а другие — нет. Это явление называется гетероплазмией и существенно затрудняет генетическую диагностику наследственного материала митохондрий.
- Тканеспецифичность. Различные ткани имеют разную степень выраженности митохондриальной дисфункции. Более того, в различных тканях (в мозге и печени, например) о нарушении работы митохондрий могут говорить различные маркеры, а изменение работы митохондрий происходит с разной скоростью. Поэтому очень трудно «перенести» данные, полученные для одного материала, на другой, и выбор оптимального материала для диагностики непрост.
- Проблема с подбором референсных значений. Определенные «границы нормы» значений для маркеров нарушения работы митохондрий разработаны только для митохондриальных заболеваний. «Норм» для возрастных изменений не существует. Для оценки степени выраженности возрастной дисфункции митохондрий необходим анализ больших баз данных.
Между тем, маркеры для оценки митохондриальной дисфункции существуют, и новые диагностические методики находятся в разработке.
Всех построим в ряд
Все существующие и потенциальные маркеры диагностики митохондриальной дисфункции можно подразделить на биохимические и генетические.
Биохимические маркеры
К этой группе методов относят определение:
А ну-ка глянем, что там?
К методам визуальной оценки относят как инвазивные методики биопсии с последующей оценкой объемной плотности митохондрий, так и неинвазивные — магнитно-резонансную спектроскопию и позитронно-эмиссионную томографию.
Небольшой укольчик
Биопсия инвазивна и дорогостояща, но она всё еще один из основных методов диагностики митохондриальных нарушений. Чаще всего проводят биопсию скелетных мышц или кожи. При подозрении на заболевание также возможна биопсия печени, миокарда. Взятый образец можно анализировать гистохимическими и иммунологическими методами, оценить количество митохондрий в образце ткани, их интактность. Кроме этого, можно выделить митохондрии и провести функциональную оценку (изучить ультраструктуру и сделать биохимический анализ дыхательной цепи).
Волшебный магнит
Про влияние питания на работу митохондрий в интернете можно найти массу информации, более или менее достоверной. Самое важное — переключиться со сжигания углеводов на жиры. Этого можно достигнуть, в первую очередь, за счет периода ночного голода не меньше 12 часов. Переедание и вызванная им «перегрузка» работой (ведь всю эту еду, в конечном счете, должны окислить митохондрии) однозначно нарушает работу митохондрий. Короткие периоды голода стимулируют динамику митохондрий , положительно влияя на системы контроля качества и работу дыхательной цепи.
Что касается витаминов, то для нормальной работы дыхательной цепи необходимо адекватное (а не избыточное!) поступление в организм цинка, магния, витаминов группы В, витаминов С и Е. При построении плана правильного питания это обязательно нужно учитывать.
На работу митохондрий также влияет ряд компонентов, входящих в БАДы (коэнзим Q, карнитин, нитраты, кофеин, альфа-липоевая кислота, таурин, мелатонин). Их эффективность подтверждена далеко не во всех случаях и сильно зависит от возрастной группы и степени дисфункции митохондрий.
Метаболиты микробиома можно разделить на группы по типу их воздействия на митохондрии:
- Оксид азота (NO) ингибирует цикл трикарбоновых кислот, снижая образование ацетил-КоА (основного энергетического субстрата) в митохондриях.
- Короткоцепочечные жирные кислоты (ацетат, пропионат и бутират). Все они, особенно бутират, являются «топливом» для дыхательной цепи митохондрий.
Может быть, стоит оказать на них влияние?
Значительная часть препаратов — потенциальных геропротекторов — оказывает воздействие на митохондрии. Рассмотрим некоторые из них.
Мишень — кардиолипин
Кардиолипин — фосфолипид, который в норме находится только во внутренней мембране митохондрий и там же синтезируется. Он состоит из четырех ацильных цепочек, которые «удерживаются» глицерином и двумя фосфатными головками (рис. 10).
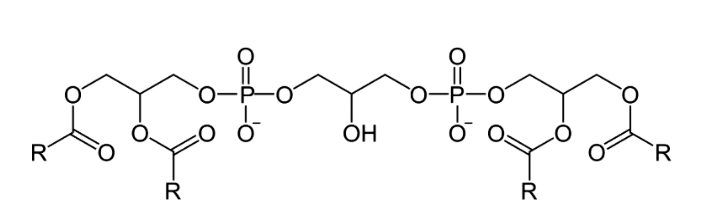
Рисунок 10. Химическая формула кардиолипина
Жирные кислоты, входящие в состав кардиолипина, различаются от ткани к ткани. В митохондриях мышц и сердца это в основном линолевая кислота. В мозге кардиолипин имеет более разнообразный жирнокислотный состав: он содержит полиненасыщенные жирные кислоты, арахидоновую и докозагексаеновую кислоты. Кардиолипин имеет уникальную коническую форму, которая агрегирует в небислойные структуры и способствует образованию крист митохондрий. Благодаря кардиолипину формируется пространственная структура внутренней мембраны, в которой комплексы дыхательной цепи сильно сближаются, формируя так называемые суперкомплексы. Благодаря этому электроны переходят от комплекса к комплексу быстрее, их утечка и образование АФК снижаются, а скорость синтеза АТФ растет.
Дефицит кардиолипина ведет к нарушению структуры крист и снижению синтеза АТФ. Ведь если связь между комплексами нарушается, и они расположены не оптимальным образом, то образование свободных радикалов усиливается, а синтез АТФ падает.
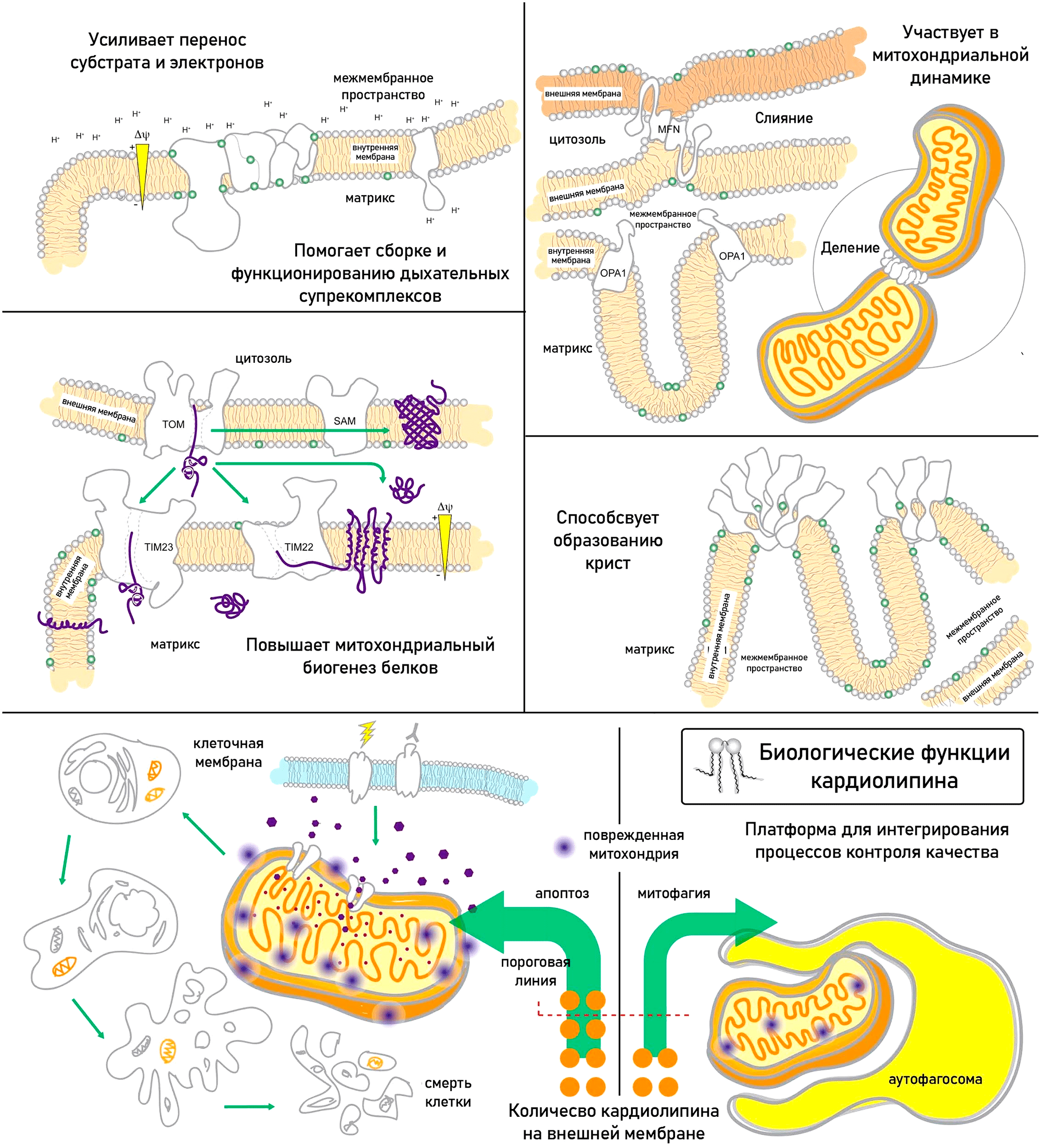
Рисунок 11. Биологические функции кардиолипина: участие в сборке и функционировании дыхательных суперкомплексов и переносе через них субстрата и электронов; участие в динамике митохондрий; повышение митохондриального биогенеза белков; участие в образовании крист митохондрий. Кроме того, кардиолипин — платформа для интегрирования процессов контроля качества митохондрий.
Неудивительно, что существенная роль кардиолипина в митохондриальных процессах и изменение его структуры с возрастом делают его интересной целью митохондриальной медицины. Подходы тут самые разные.
Помимо фосфолипидов-предшественников, есть еще коммерческий фармакологический препарат эламипретид. Он поглощается клетками при помощи пассивной диффузии, проникая даже в деполяризованные митохондрии, и взаимодействует с кардиолипином. In vitro было показано, что эламипретид оказывает на организм следующее воздействие:
- снижает образование АФК;
- повышает уровень поглощения кислорода;
- снижает окисление кардиолипина;
Эламипретид сейчас проходит клинические испытания второй фазы (NCT02805790, NCT02693119, NCT02976038). Недавно две компании: Stealth BioTherapeutics (специализация — митохондриальные заболевания) и Alexion Pharmaceuticals (специализация — редкие заболевания) подписали соглашение для совместной разработки и коммерциализации этого препарата.
Скажи «нет» окислению!
Если раньше, согласно теории Хармана, АФК считали главной причиной старения и всевозможных повреждений, то сейчас мы знаем, что это не совсем так.
Сегодня известно, что АФК — это не столько «зло», сколько сигнал к действию. И только когда организм не может отреагировать на этот сигнал должным образом (усилив антиоксидантную защиту, устранив поврежденные митохондрии, обеспечив работающие митохондрии недостающими им белками) — только тогда свободные радикалы становятся орудием массового поражения, что приводит к окислительному стрессу, воспалению и старению. У здоровых людей использование антиоксидантов может снижать показатели адаптации к спортивным нагрузкам. Поэтому их эффективность для улучшения состояния организма в значительной мере зависит от выбранной целевой группы.
Для нейтрализации АФК в организме существуют различные системы антиоксидантной защиты (эндогенные антиоксиданты). Но как бы ни совершенна была наша клеточная система антиоксидантной защиты, иногда ее оказывается недостаточно для предотвращения развития окислительного стресса и воспаления. Тогда возможно использование экзогенных антиоксидантов. Несмотря на то, что свободнорадикальная теория старения была пересмотрена, поиск новых антиоксидантов и оптимизация их работы всё еще находятся в топе биотехнологических исследований в митохондриальной медицине, и антиоксиданты представляют собой наиболее обширную группу препаратов, используемых при терапии дисфункции митохондрий.
Необходимо отметить, что понятие «антиоксиданты» очень широкое. К ним относятся совершенно разные соединения и молекулы, которые способны:
- усиливать естественные системы антиоксидантной защиты;
- снижать утечку электронов и уровень образования АФК;
- непосредственно нейтрализовать АФК, связываясь с ними.
Антиоксиданты могут снижать окислительный стресс, но они не влияют на производство АТФ и работу дыхательной цепи. Они могут действовать как в цитоплазме (например витамин С), так и в липидной фракции мембран (витамин Е). Так как митохондрии в клетке являются основным местом образования АФК, то разрабатываются также таргетные антиоксиданты, действие которых направлено непосредственно на митохондрии.
К группе таргетных антиоксидантов относятся SkQ (ионы Скулачева) и MitoQ. Они могут проходить через двойную мембрану митохондрий, воздействуя непосредственно в месте образования свободных радикалов — вблизи ЭТЦ. Молекула SkQ состоит из двух частей: челнока, который протаскивает ее через мембрану митохондрий, и антиоксиданта пластохинона (растительного аналога убихинона, или коэнзима Q10).
Препарат MitoQ по своему механизму действия очень сходен с SkQ. Молекула митохинона (MitoQ) состоит из переносчика через митохондриальную мембрану и убихинона. Однако оба эти соединения не проникают в деполяризованные митохондрии, так как их способность проходить через митохондриальную мембрану напрямую зависит от ее заряда.
Главный эффект ангиотензина — сужение сосудов. Так как это влияет на количество кислорода, то логично предположить, что митохондрии как основные потребители кислорода должны как-то реагировать на изменение количества ангиотензина. И правда, недавно обнаружили, что у митохондрий есть два класса рецепторов к ангиотензину — АТ1 и АТ2. При этом в зависимости от того, с каким из рецепторов свяжется ангиотензин, действие его разнится. Активация АТ2 приводит к снижению митохондриального дыхания и повышению концентрации оксида азота. Эти эффекты защищают от окислительного стресса и вызванного им повреждения. А вот активация АТ1, наоборот, приводит к образованию супероксида и окислительному стрессу. Уровень производства «хороших» рецепторов АТ2 существенно выше, а окислительный стресс приводит к дополнительному компенсаторному усилению их активности.
А если подправить гены?
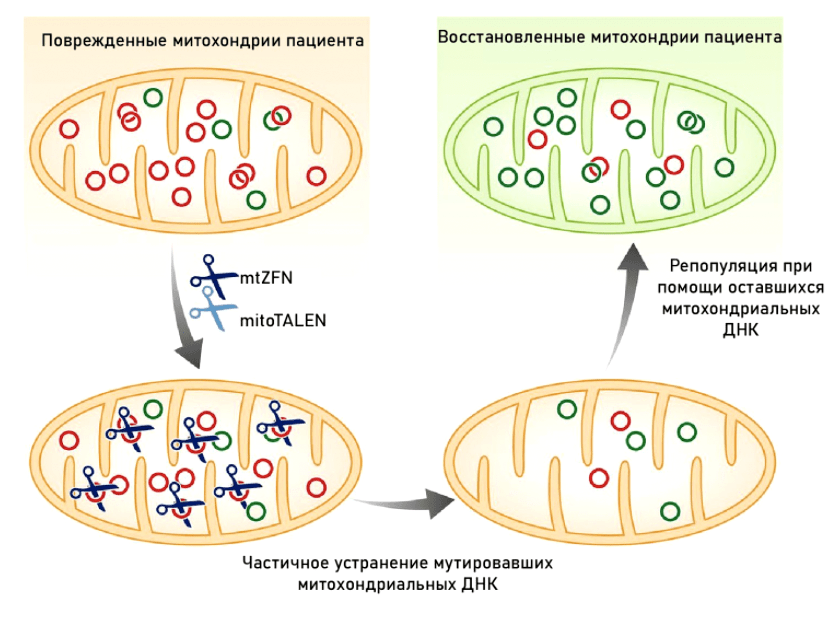
Рисунок 12. Принцип действия генной терапии митохондрий: направленное повреждение мутантных копий мтДНК с последующей репликацией здоровых копий
Именно поэтому практически все методы генной терапии митохондрий направлены не на коррекцию мутантных генов, а на прицельную деградацию ДНК в митохондриях с мутацией, что изменяет соотношение гетероплазмии в сторону немутантных. Данное направление генной терапии носит название «антигеномное», или «антирепликативное».
В нем различают несколько методических подходов, которые мы коротко опишем с указанием их основных преимуществ и недостатков.
Использование ДНК-нуклеаз
Недостаток этого метода — сложность в поиске той последовательности-мишени, которая будет присутствовать только в мутантных митохондриях, но не в здоровых. Для более чем двухсот мутаций мтДНК, ассоциированных с заболеваниями, только у двух была обнаружена та единственная и неповторимая последовательность ДНК, подходящая в качестве мишени для нуклеаз.
Создание Zn-finger ДНК-связывающихся модулей (mitoZFN)
Инженерные «цинковые пальцы» (zinc finger nucleases, ZFNs) — это химерные ферменты, содержащие две структурные единицы: связывающуюся со строго определенной последовательностью ДНК и расщепяющую ее. Этот метод широко использовался и для редактирования ядерных геномов, но был вытеснен CRISPR-Cas-технологией. А вот для митохондриального геномного редактирования он по-прежнему применяется на клеточных и животных моделях митохондриальных заболеваний.
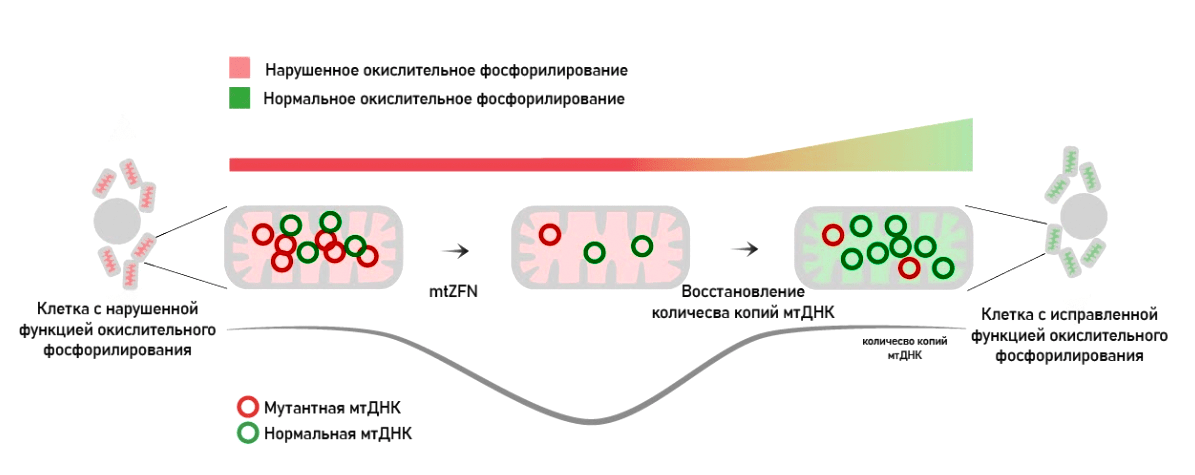
Рисунок 13. Генная терапия митохондрий при помощи «цинковых пальцев», разрушающих мутантные копии митохондриальной ДНК, снижая гетероплазмию
Такие модули «цинковых пальцев» были созданы для практически всех шестидесяти четырех нуклеотидных комбинаций кодонов. Для удобства распознавания и последующего удаления к такому модулю можно добавить специфический «флажок», облегчающий распознавание нужной последовательности — метильную метку. В данном случае это может делать метилтрансфераза DNMT3. Такой нуклеотид будет гораздо проще распознать. Благодаря этому комбинация (модуль mitoZFN, направленный на какую-то последовательность, плюс генный конструкт со специфической нуклеазой) позволяет таргетно убирать специфические последовательности мтДНК.
Интересно, что синтез нескольких комбинаций специфичных mtZFNs-модулей использовалась также для удаления «частой делеции» 4977-bp (о которой мы говорили выше) на модели цитоплазматических гибридов клеток. Данная делеция ассоциирована с офтальмоплегией и накапливается у всех людей в процессе старения в различных тканях.
Сложность данного метода в том, что большое количество модулей внутрь митохондрии доставить достаточно сложно.
MitoTALENs (transcription activator-like effector nucleases)
Основной недостаток этого метода — сложность доставки большого количества TALEN внутрь митохондрии, так как вектор может быть слишком большой.
Редактирование генома при помощи системы CRISPR-Cas9
Что касается редактирования митохондриального генома, то тут возникают сложности, так как, во-первых, довольно сложно доставить направляющую РНК внутрь митохондрии, что необходимо для нацеливания белка Cas9. Во-вторых, в митохондриях низкий уровень репарационных процессов, отвечающих за восстановление двунитевых разрывов. При редактировании же генома результат работы CRISPR-Cas9 — это починка двухцепочечного разрыва, произведённого Cas9. С низким уровнем репарации этот процесс протекает довольно сложно.
Общий недостаток всей этой группы методов генного редактирования (а по сути — удаления копий мтДНК, несущих мутацию) — возможность снизить общее количество мтДНК ниже функционального порогового уровня. Это усугубляет проблему митохондриальной дисфункции и может привести к апоптозу клетки.
Митохондрии и психика
Когда мышь испытывает психологический стресс, ее Т-клетки активируются, а митохондрии фрагментируются так же, как если бы ее организм столкнулся с вирусом. Если же создать таких мышей, Т-клетки которых всегда активны, а митохондрии — фрагментированы, они будут тревожными, заторможенными, нелюбопытными и лишенными всякой мотивации. А это уже классическая депрессивная симптоматика. Что ставит перед учеными новый вопрос: что, если митохондрии виноваты в проблемах с настроением у человека?
Чтобы проверить гипотезу, исследователи заставили крыс конкурировать за социальную иерархию. Доминирующие позиции заняли животные с меньшим уровнем тревожности. Потом ученые изучили митохондрии прилежащего ядра мозга крыс — отдела, который регулирует эмоции и поведение что у грызунов, что у людей. Оказалось, у крыс-аутсайдеров митохондрии функционируют хуже. А еще в них меньше белков для превращения кислорода и глюкозы в энергию — то есть не хватает оборудования, чтобы митохондрия работала эффективно. Различие оказалось врожденным.
Неизвестно, делают ли нас, людей, тревожными и депрессивными врожденные особенности митохондрий так же, как и грызунов. Но на стресс митохондрии человека реагируют тем же образом. В одном эксперименте, например, людей подвергли стрессу: обвинили в краже или нарушении ПДД — и заставили за две минуты продумать стратегию защиты. В крови участников увеличилось количество митохондриальной ДНК, которая активировала иммунную реакцию, — совсем как в случае с мышами.
Как можно помочь своим митохондриям
Некоторые изменения в образе жизни, и прием полезных веществ также могут увеличить число митохондрий в клетке.
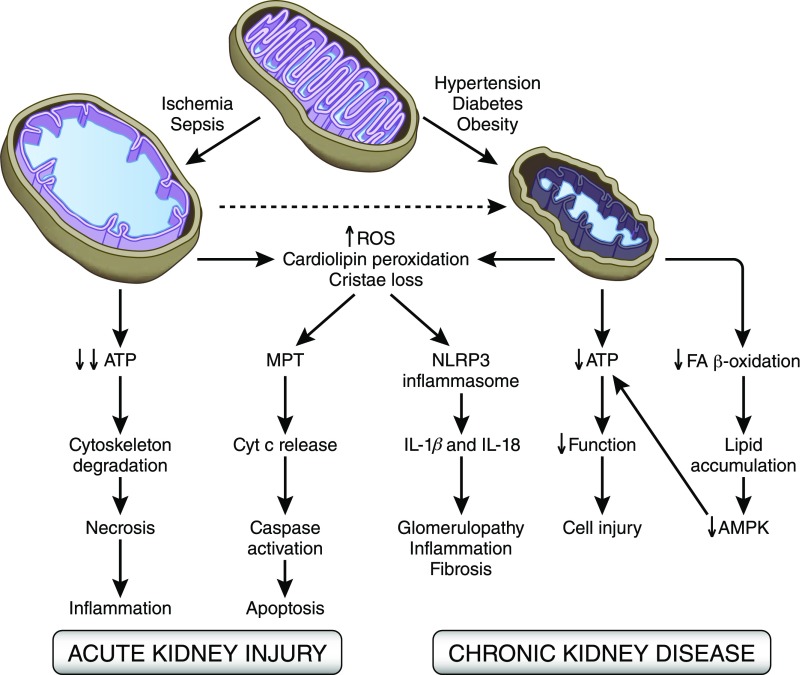
ИЗМЕНЕНИЯ В РАБОТЕ МИТОХОНДРИЙ ПРИ ЗАБОЛЕВАНИИ ПОЧЕК (www.ncbi.nlm.nih.gov)







